
| A、原溶液一定不存在较大浓度的H+、Mg2+ |
| B、原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5:2:1 |
| C、不能确定原溶液是否含有K+、NO3- |
| D、实验中产生的棕色气体遇空气颜色会加深 |
| 3.08g |
| 154g/mol |
| 1.0g |
| 100g/mol |
| 3.08g |
| 154g/mol |


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu溶于稀HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O |
| B、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ |
| C、用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
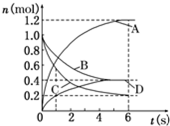 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A、反应进行到6 s时,各物质的反应速率相等 |
| B、反应进行到1 s时,v (A)=v (C) |
| C、反应进行到6 s时,B的平均反应速率为0.1 mol/(L?s) |
| D、该反应的化学方程式为3B+4C?6A+2D |
查看答案和解析>>
科目:高中化学 来源: 题型:
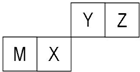
| A、M的离子半径小于Z的离子半径 |
| B、M和Y的最高价氧化物对应水化物之间能相互反应 |
| C、X的单质可以做光导纤维和半导体材料 |
| D、常温下,0.01mol/L的Y的气态氢化物的水溶液的pH=12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽车尾气中的NOx是造成光化学烟雾的唯一因素 |
| B、空气中SO2、NOx等是形成酸雨的重要原因 |
| C、冬天撒盐熔雪能造成土壤和水污染 |
| D、河流人海口处形成的三角洲是海水使河水泥沙胶体凝聚的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
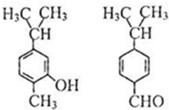
| A、不是同分异构体 |
| B、分子中共平面的碳原子数相同 |
| C、均能与溴水反应 |
| D、可用红外光谱区分,但不能用核磁共振氢谱区分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com