
| A. | ①② | B. | ②③ | C. | ③④ | D. | ① |
分析 ①苯燃烧时发生明亮并带有浓烟的火焰,是含碳量高的原因;
②发生加成反应是不饱和键具有的性质,不饱和烃能与H2发生加成反应;
③苯中不含碳碳双键,因此不能被酸性高锰酸钾溶液氧化,不能与溴发生加成反应;
④苯分子具有平面正六边形结构,其中6个碳原子之间的键完全相同.
解答 解:①苯燃烧时发生明亮并带有浓烟的火焰,是因为苯分子中含碳量高,乙烯燃烧时发生明亮并带有黑烟的火焰,不能说明苯分子没有与乙烯类似的双键,故①错误;
②苯能在一定条件下跟H2加成生成环己烷,发生加成反应是双键具有的性质,不能说明苯分子没有与乙烯类似的双键,故②错误;
③苯不因化学变化而使溴水褪色,说明苯分子中不含碳碳双键,苯不与酸性高锰酸钾溶液或溴水发生反应,能说明苯分子没有与乙烯类似的双键,故③正确;
④若苯中含碳碳双键,则苯分子不可能为平面正六边形结构,而苯是平面正六边形结构,说明其中6个碳原子之间的键完全相同,是介于碳碳单键、碳碳双键之间的一种特殊化学键,并无碳碳双键,故④正确;
故选C.
点评 本题考查了苯与烯烃结构的区别和性质的差异,题目难度不大,掌握苯的结构和性质是解题的关键,平时学习时注意不同类物质结构和性质的比较.


科目:高中化学 来源: 题型:解答题
 )2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(
)2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林( ,M=180)和Cu2+;
,M=180)和Cu2+;| 阿司匹林溶解质量 | 阿司匹林铜的溶解质量 | |
| 氯仿 | 0.4g | 不溶 |
| 无水乙醇 | 0.9g | 不溶 |
| 蒸馏水 | 不溶 | 不溶 |
| 实验编号 | 阿司匹林:无水硫酸铜/物质的量之比 | 产率% | ||
| X1 | X2 | 平均值 | ||
| 1 | 1:1 | 76.6 | 78.1 | 77.4 |
| 2 | 2:1 | 78.6 | 75.1 | 76.8 |
| 3 | 3:1 | 93.9 | 95.9 | 94.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | NH3+HCl═NH4Cl | ||
| C. | 2 NaOH+SO2═Na2SO3+H2O | D. | AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.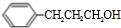

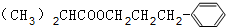 +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
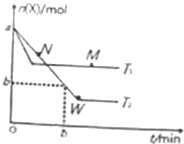 在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )
在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )| A. | 正反应方向为放热反应 | |
| B. | 在T2温度下,在0~t1时间内,v(Y)=$\frac{a-b}{{t}_{1}}$mol•(L•min)-1 | |
| C. | M点的正反应速率v(正)大于N点的逆反应速率v(逆) | |
| D. | W点时再加入一定量X,平衡后X的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com