
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子氧化性:A(n+1)+>Bn+离子还原性:C(n+1)->Dn- | |
| D. | 单质还原性:A>B,单质氧化性:D>C |
分析 已知aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,结合元素周期律递变规律解答该题.
解答 解:A.aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则有:a-n-1=b-n=c+n+1=d+n,则有A、B在周期表中C、D的下一周期,并且原子序数:a>b>d>c,故A错误;
B.具有相同电子层结构的离子,原子序数大的离子半径小,则离子半径大小为:C(n+1)->Dn->Bn+>A(n+1)+,故B错误;
C.金属性越强,对应离子的氧化性越弱,非金属性越强,对应离子的还原性越强,则离子还原性为:C(n+1)->Dn-,离子氧化性为Bn+<A(n+1)+,故C正确;
D.同周期从左向右金属的还原性减弱,单质的氧化性增强,则单质还原性为B>A,单质氧化性为D>C,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,明确核外电子排布确定元素所在周期表中的位置以及把握元素周期律的递变规律是解答该题的关键,试题培养了学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 该元素的相对原子质量的近似值一定是(m+n) | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | 若12C的质量为Wg,则该原子的质量约为(m+n)Wg | |
| D. | 若NA表示阿伏加德罗常数,则该原子的摩尔质量为(m+n)•NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数和气体质量均不同 | B. | 分子数和中子数均相同 | ||
| C. | 质子数和中子数均相同 | D. | 分子数、原子数和质子数均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | N原子的第一电离能大于O原子 | N原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C=O之间的夹角为120° |
| C | H2O的沸点大于H2S的沸点 | H2O是液态的,H2S是气态的 |
| D | HF比HCl稳定 | HF分子间可以形成氢键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )| A. | ①②③ | B. | ①③② | C. | ②①③ | D. | ②③① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
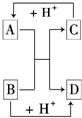 已知A、B、C、D是中学化学中常见的四种不同粒子.它们之间存在如图所示的转化关系.
已知A、B、C、D是中学化学中常见的四种不同粒子.它们之间存在如图所示的转化关系.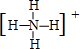 ,D的电子式
,D的电子式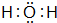 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
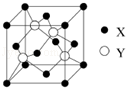 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 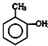 甲基苯酚 甲基苯酚 | |
| B. | 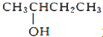 2-羟基丁烷 2-羟基丁烷 | |
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| D. | CH2=CH-CH=CH-CH=CH2 1,3,5-己三烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com