
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I反应产物的定性探究
按下图装置(固定装置已略去)进行实验
(1)A中反应的化学方程式为:
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
实验Ⅱ 反应产物的定量探究
(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:
资料2:X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。
仅由上述资料可得出的正确结论是 。
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度≥15 mol·L-1
d.硫酸浓度越大,黑色物质越快出现、越难消失
(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol·L-1Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为ag,则硫酸铜的产率为 。 (已知:2Cu2++4I-=2CuI+I2,2S2O32-+I2=S4O62-+2I-)
(14分)(1) Cu +2H2SO4(浓)= CuSO4 + SO2+ 2H2O (2分)
(2)NaOH溶液(或KMnO4溶液等) (2分)
(3)D装置中黑色固体颜色无变化,E中溶液褪色 (2分)
(4)将A装置中试管内冷却的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌 (2分)
(5)使用上述装置,不放入铜丝进行实验,观察无水硫酸铜是否变蓝 (2分)
(6)abd
(7)(64bV/a)% (2分)
解析试题分析:⑴铜与浓硫酸的反应Cu +2H2SO4(浓)  CuSO4 + SO2↑+ 2H2O,故答案为:Cu +2H2SO4(浓)
CuSO4 + SO2↑+ 2H2O,故答案为:Cu +2H2SO4(浓)  CuSO4 + SO2↑+ 2H2O;⑵F为尾气吸收装置,通常用NaOH溶液或KMnO4溶液,答案:NaOH溶液(或KMnO4溶液等);⑶如果有H2产生,则D中固体变红,E溶液不褪色,所以如产生SO2,则D装置中黑色固体颜色无变化,E中溶液褪色,证明浓硫酸中硫元素的氧化性强于氢元素。答案:D装置中黑色固体颜色无变化,E中溶液褪色;⑷含有Cu2+ 的稀溶液的颜色为蓝色,所需的操作是将含浓硫酸的混合溶液稀释。答案:将A装置中试管内冷却的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌。⑸控制反应条件,使反应不产生SO2,进行对比实验。答案:使用上述装置,不放入铜丝进行实验,观察无水硫酸铜是否变蓝。⑹a正确,反应中有黑色的固体产生,生成物不止一种,反应不止一个;b从资料1的表中看出浓硫酸浓度在16mol/L以下时,加热后黑色的固体可能消失,b正确;c反应只要是浓硫酸,资料中没有强调硫酸浓度≥15 mol·L-1,c不正确;d从表中看出.硫酸浓度越大,黑色固体出现的温度越低,黑色物质越快出现、消失所需温度越高,甚至不消失,d正确,选a b d.。
CuSO4 + SO2↑+ 2H2O;⑵F为尾气吸收装置,通常用NaOH溶液或KMnO4溶液,答案:NaOH溶液(或KMnO4溶液等);⑶如果有H2产生,则D中固体变红,E溶液不褪色,所以如产生SO2,则D装置中黑色固体颜色无变化,E中溶液褪色,证明浓硫酸中硫元素的氧化性强于氢元素。答案:D装置中黑色固体颜色无变化,E中溶液褪色;⑷含有Cu2+ 的稀溶液的颜色为蓝色,所需的操作是将含浓硫酸的混合溶液稀释。答案:将A装置中试管内冷却的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌。⑸控制反应条件,使反应不产生SO2,进行对比实验。答案:使用上述装置,不放入铜丝进行实验,观察无水硫酸铜是否变蓝。⑹a正确,反应中有黑色的固体产生,生成物不止一种,反应不止一个;b从资料1的表中看出浓硫酸浓度在16mol/L以下时,加热后黑色的固体可能消失,b正确;c反应只要是浓硫酸,资料中没有强调硫酸浓度≥15 mol·L-1,c不正确;d从表中看出.硫酸浓度越大,黑色固体出现的温度越低,黑色物质越快出现、消失所需温度越高,甚至不消失,d正确,选a b d.。
⑺ 根据方程式2Cu2++4I-=2CuI+I2,2S2O32-+I2=S4O62-+2I-,
得关系式Cu2+ ― S2O32―
c×25 bv
n(Cu2+ )=
则硫酸铜的产率为:实际产量÷理论产量×100%=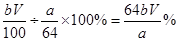
考点:元素化合物知识、基本实验实验、化学反应原理、氧化还原反应、化学计算等综合性较强。中等难度。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:填空题
辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
⑴写出浸取过程中Cu2S溶解的离子方程式:____________________。
⑵回收S过程中温度控制在50~60℃之间,不宜过高或过低的原因是_____________。
⑶气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为___________________________;向滤液M中加入(或通入)下列__________(填字母)物质,得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
⑷保温除铁过程中,加入CuO的目的是________________________;蒸发浓缩时,要用HNO3溶液调节溶液的pH,其理由是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
叠氮化钠(NaN3)是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起。实验室测定叠氮化钠样品中NaN3的质量分数。实验步骤如下:
①称取约2.5000g叠氮化钠试样,配成250mL溶液。
②准确量取25.00mL溶液置于锥形瓶中,用滴定管加入50.00mL 0.1000mol·L-1
(NH4)2Ce(NO3)6(六硝酸铈铵),
[发生反应为:2(NH4)2Ce(NO3)6 +2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质不参与反应)。
③反应后将溶液稍稀释,然后向溶液中加入5mL浓硫酸,滴入2滴邻菲哕啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2(硫酸亚铁铵)标准滴定溶液滴定过量的Ce4+至溶液由淡绿色变为黄红色(发生的反应为:Ce4++Fe2+= Ce3++Fe3+),消耗硫酸亚铁铵标准溶液24.00mL。
(1)步骤①配制叠氮化钠溶液时,除需用到烧杯、玻璃棒、量筒外,还用到的玻璃仪器有 、 。
(2)叠氮化钠受撞击时生成两种单质,反应的化学方程式为 。
(3)若其它读数正确,滴定到终点后,读取滴定管中 (NH4)2Fe(SO4)2标准溶液体积按图图示读取,将导致所测定样品中叠氮化钠质量分数 (选填:“偏大”、“偏小”或“不变”)。
(4)通过计算确定叠氮化钠试样中含NaN3的质量分数为多少(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某研究性学习小组利用H2还原法测定两种铜的氧化物CuO、Cu2O混合粉末中铜元素的质量分数。下图是测定装置的示意图,A中的试剂是盐酸。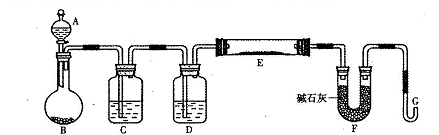
请回答下列问题。
(1)烧瓶中装入的试剂是锌粒,其中将发生反应的离子方程式是 ;
(2)试剂C是水,其作用是__ __;
(3)试剂D是__ __,其作用是干燥氢气;
(4)连接好装置后的实验操作依次是_ __(填下列操作序号)
①检验氢气纯度;②加热E;③检验装置气密性;④点燃G管溢出的气体;⑤从A瓶逐滴滴加液体
(5)已知:C(s)+1/2O2( g)= CO(g) △H=-110.5kJ·mol-1,
Cu2O(s) +1/2O2(g) = 2CuO(s) △H=-145 kJ·mol-1
则用炭粉在高温条件下还原CuO生成Cu2O的热化学方程式:____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学在气体体积测定仪中用镁和硫酸反应测定1 mol氢气体积。完成下列填空:
(1)A中发生反应的离子方程式为______________________。
(2)检查装置气密性的方法是塞上B瓶的玻璃塞,用橡皮塞塞紧A瓶加料口,当看到__________________现象时,可以确认装置气密性良好。
(3)已知液体量瓶的刻度范围是110~130 mL,实验时称取镁带的质量要控制在0.100~0.110 g之间,目的是_________。
(4)完成一次测定实验,需要2次用注射器抽气,其中需要记录的是第__________次抽出气体的体积。
(5)下列情况会导致实验结果偏高的是______(填编号)
a. 镁表面的氧化膜没有除尽 b. 储液瓶中的液体是水
c. 未冷却到室温就读数 d. 装置气密性不好
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
下面是一些实验室制备硫酸铜的实验设计。
实验一:用铜与浓硫酸反应制取硫酸铜。
实验二:将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全制取硫酸铜。(装置如下图中的图I.图Ⅱ)。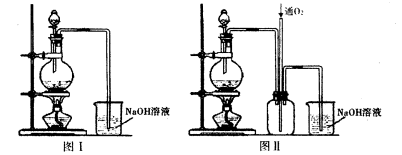
实验三:将铜粉在某仪器中反复灼烧,使铜粉充分与空气发生反应生成氧化铜,再将氧化铜与稀硫酸反应,经后续步骤可得到硫酸铜晶体。
实验四:向铜粉和稀硫酸的混合物中加入H2O得到硫酸铜。
请回答实验中的有关问题。
(1)实验一中发生反应的化学反应方程式为____,这种方法的缺点是____。
(2)实验二装置图中分液漏斗里盛装的液体是____。图Ⅱ是图I的改进装置,分析图II装置的优点是 。
(3)实验三中用于灼烧的仪器名称是 。该实验中的后续步骤指的是__ 。
(4)实验四中发生反应的化学方程式为____。
(5)除上面的实验设计外,请你再设计一种只用铜和稀硫酸为原料制取硫酸铜的方法(写出化学反应方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
(1)装置乙的作用是_____________________。
(2)装置丁的作用是吸收污染空气的SO2气体,其反应的离子方程为 。
(3) SO2 气体有漂白性、还原性和氧化性。将SO2 通入氯水中,SO2表现的是________性,化学反应方程式为 。
(4)反应过程中,将丙中滴管里的品红溶液滴入锥形瓶,若现象为 ,则溶液中的NaOH完全转化为了NaHSO3。
(5)若丙中没有加入品红溶液,则不能准确判断氢氧化钠是否完全转化。现有可供选择的仪器和试剂:烧杯、试管、玻璃棒、胶头滴管; 2 mol/L盐酸、2 mol/L硝酸、1 mol/L氯化钡溶液、l mol/L氢氧化钡溶液、品红溶液、蒸馏水。
请设计实验探究吸收后产物中是否存在NaHSO3 和Na2SO3,将实验操作、预期的实验现象和结论填在下表中。
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量待测液放入试管中,滴加过量lmol/L氯化钡溶液。静置一段时间后,得到滤液A和固体B。 | |
| 步骤2:往固体B中加入蒸馏水洗涤沉淀,静置后弃去上层清液,向固体滴入2滴(或少量)品红,再 | 若品红褪色(或有气泡),则 |
| 步骤3: | 若 则 ; 否则 。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(1)在硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行
次。
(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(3)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。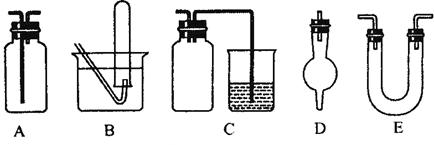
请回答下列问题:
①能用作干燥氨气的装置有_______________(填字母);
②既能用于收集氯气又能用于收集一氧化氮气体的装置有_______________(填字母);
③在实验室制备氯气的实验中,用以除去氯气中氯化氢等杂质气体的装置有________________ (填字母);
④能用于乙烯与溴水反应制二溴乙烷的实验装置有__________(填字母);
⑤在C装置中,若用烧杯内的氢氧化钠溶液吸收尾气二氧化硫,则广口瓶的作用是___________________。
(4)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了右图所示的实验。
①可通过观察 来定性的得出结论;
②有A同学提出将CuSO4改为CuCl2更为合理,其理由是 ;
若不采用A同学的改进方案,你认为还可以如何改进? 。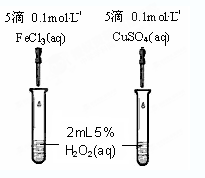
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com