

·ÖĪö £Ø1£©¢ŁĶÓėÅØĮņĖį·“Ӧɜ³É¶žŃõ»ÆĮņŗĶĮņĖįĶ£»
¢Śæ¼ĀĒ¶žŃõ»ÆĮņĪŪČ¾»·¾³ŗĶÅØĮņĖįĄūÓĆĀŹ£»
£Ø2£©Fe2+Äܱ»ŃõĘųŃõ»Æ£»
£Ø3£©¢ŁŅõĄė×ÓŅĘĻņÓŚŃō¼«£¬Ńō¼«ĪŖĶʬ£»
¢ŚĢę»»ĪŖNa2SO4ŗó£¬Ņõ¼«Ēų·¢Éś·“Ó¦2H++2e-=H2”ü£¬Ņõ¼«Ēųc£ØOH-£©£¾c£ØH+£©£¬pHÉżøߣ®
½ā“š ½ā£ŗ£Ø1£©¢ŁCuÓėÅØĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£»
¢ŚøĆ·½·Ø·“Ó¦²śÉśSO2£¬¶Ō»·¾³ÓŠĪŪČ¾»ņŃõ»Æ¼ĮÅØĮņĖįĄūÓĆĀŹ²»øߣ»
¹Ź“š°øĪŖ£ŗ·“Ó¦²śÉśSO2£¬¶Ō»·¾³ÓŠĪŪČ¾»ņŃõ»Æ¼ĮÅØĮņĖįĄūÓĆĀŹ²»øߣػņĘäĖūŗĻĄķ“š°ø£©£»
£Ø2£©Éś³ÉµÄŃĒĢśĄė×Ó±»ŃõĘųŃõ»Æ£¬4Fe2++O2+4H+=4Fe3++2H2O£»
¹Ź“š°øĪŖ£ŗ4Fe2++O2+4H+=4Fe3++2H2O£»
£Ø3£©¢ŁÓÉĶ¼æÉÖŖĮņĖįøłĄė×ÓŅĘĻņÓŚa¼«Ņ»¶Ė£¬ŌņaĪŖŃō¼«£¬Ź§µē×ÓŅ»¼«£¬µē½āµÄ·½·ØÖĘCuSO4£¬ĖµĆ÷ĶŹ§µē×ÓµĆĶĄė×Ó£¬Ōņa¶ĖĻąĮ¬µÄµē¼«²ÄĮĻŹĒĶʬ£»
¹Ź“š°øĪŖ£ŗĶʬ£»
¢ŚĢę»»ĪŖNa2SO4ŗó£¬Ņõ¼«Ēų·¢Éś·“Ó¦2H++2e-=H2”ü£¬Ņõ¼«Ēųc£ØOH-£©£¾c£ØH+£©£¬OH-Ņ²æÉŅŌĶعżŅõĄė×Ó½»»»Ä¤ŌĖ¶Æµ½Ńō¼«Ēų£¬µ¼ÖĀCuSO4ČÜŅŗpHÉżøߣ»
¹Ź“š°øĪŖ£ŗĢę»»ĪŖNa2SO4ŗó£¬Ņõ¼«Ēų·¢Éś·“Ó¦2H++2e-=H2”ü£¬Ņõ¼«Ēųc£ØOH-£©£¾c£ØH+£©£¬OH-Ņ²æÉŅŌĶعżŅõĄė×Ó½»»»Ä¤ŌĖ¶Æµ½Ńō¼«Ēų£¬µ¼ÖĀCuSO4ČÜŅŗpHÉżøߣ®
µćĘĄ ±¾Ģāæ¼²éĮĖĮņĖįĶµÄÖʱø£¬µē½āŌĄķµÄ·ÖĪöÓ¦ÓĆ£¬Ö÷ŅŖŹĒŃõ»Æ»¹Ō·“Ó¦µÄÓ¦ÓĆ£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśÓėŃĪĖį·“Ó¦£ŗ2Fe+6H+=2Fe3++3H2”ü | |
| B£® | Ģ¼ĖįĒāÄĘČÜŅŗÓėĻ”ŃĪĖį»ģŗĻ£ŗHCO3-+H+=H2O+CO2”ü | |
| C£® | ĮņĖįĶČÜŅŗÓėĒāŃõ»ÆÄĘČÜŅŗ»ģŗĻ£ŗCuSO4+2OH-=Cu£ØOH£© 2”ż+SO42- | |
| D£® | ĻõĖįŅųČÜŅŗÓėĀČ»ÆÄĘČÜŅŗ»ģŗĻ£ŗAgNO3+Cl-=AgCl”ż+NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł»ņ¢Ś | B£® | ¢Ś»ņ¢Ü | C£® | ¢Ł»ņ¢Ū | D£® | ¢Ū»ņ¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶µÄ“óŠ”Ė³Šņ£ŗr£ØY£©£¾r£ØZ£©£¾r£ØW£© | |
| B£® | ŌŖĖŲZ”¢WµÄ¼ņµ„Ąė×ӵĵē×Ó²ć½į¹¹ĻąĶ¬ | |
| C£® | ŌŖĖŲY µÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČZ µÄĒæ | |
| D£® | Ö»ŗ¬X”¢Y”¢ZČżÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬Ņ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
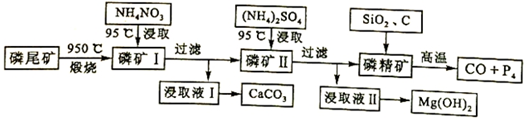
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ā×ĒŁ | B£® | Ā¬ÉŖø£ | C£® | µĄ¶ū¶Ł | D£® | ĢĄÄ·Ėļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
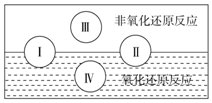 Ńõ»Æ»¹Ō·“Ó¦ŌŚÉś²ś”¢Éś»īÖŠ¾ßÓŠ¹ć·ŗµÄÓĆĶ¾£¬¹į“©¹Å½ń£®
Ńõ»Æ»¹Ō·“Ó¦ŌŚÉś²ś”¢Éś»īÖŠ¾ßÓŠ¹ć·ŗµÄÓĆĶ¾£¬¹į“©¹Å½ń£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ·“Ó¦¢ń£ŗ”÷H£¾0£¬p2£¾p1 | B£® | ·“Ó¦¢ō£ŗ”÷H£¼0£¬T2£¾T1 | ||
| C£® | ·“Ó¦¢ó£ŗæÉÄÜŹĒ”÷H£¾0£¬T2£¾T1 | D£® | ·“Ó¦¢ņ£ŗ”÷H£¼0£¬T1£¼T2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com