
【题目】置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题: 
(1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,则该反应的离子反应方程式为
(2)工业上利用置换反应原理制备一种半导体材料,写出该反应的化学方程式
(3)若气体单质乙能在空气中燃烧,化合物B为黑色磁性晶体,写出该反应的化学方程式 .
【答案】
(1)2Na+2H2O=2Na++2OH﹣+H2↑
(2)SiO2+2C ![]() Si+2CO↑
Si+2CO↑
(3)3Fe+4H2O(g) ![]() Fe3O4+4H2
Fe3O4+4H2
【解析】解:(1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,A为水,甲为Na,生成B为NaOH,该反应的离子反应方程式为2Na+2H2O=2Na++2OH﹣+H2↑,
所以答案是:2Na+2H2O=2Na++2OH﹣+H2↑;(2)工业上利用置换反应原理制备一种半导体材料,为C与二氧化硅反应生成Si、CO,该反应为SiO2+2C ![]() Si+2CO↑,
Si+2CO↑,
所以答案是:SiO2+2C ![]() Si+2CO↑;(3)若气体单质乙能在空气中燃烧,化合物B为黑色磁性晶体,B为四氧化三铁,则甲为Fe,A为水蒸气,该反应为3Fe+4H2O(g)
Si+2CO↑;(3)若气体单质乙能在空气中燃烧,化合物B为黑色磁性晶体,B为四氧化三铁,则甲为Fe,A为水蒸气,该反应为3Fe+4H2O(g) ![]() Fe3O4+4H2,
Fe3O4+4H2,
所以答案是:3Fe+4H2O(g) ![]() Fe3O4+4H2.
Fe3O4+4H2.


科目:高中化学 来源: 题型:
【题目】现有①汽车;②机器上的齿轮;③门把手;④锯条;⑤铁制洗脸盆等常见铁制品。为了防止它们生锈,通常适合采用下面哪一种方法。(填序号)
(1)在表面喷漆;
(2)在表面涂油;
(3)在表面镀一层其他金属;
(4)在表面烧制搪瓷;
(5)使其表面形成致密的氧化物保护膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)![]() 系统命名法为 ,
系统命名法为 ,
(2)4﹣甲基﹣1﹣戊烯的键线式为 ,
(3)写出乙醛与新制氢氧化铜反应化学方程式 ,
(4)下列有关实验的说法不正确的是 . A.制乙烯时,温度计应插入反应混合液中
B.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液
C.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤
D.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氢硅(SiHCl3)是生产多晶硅的主要原料.由粗硅制三氯氢硅的反应如下:
反应的热化学方程式 | 平衡常数(300℃) | |
主反应 | Si(s)+3HCl(g)SiHCl3(g)+H2(g)△H=﹣210kJmol﹣1 | K1(molL﹣1)﹣1 |
副反应 | Si(s)+4HCl(g)SiHCl4(g)+2H2(g)△H=﹣240kJmol﹣1 | K2(molL﹣1)﹣1 |
回答下列问题:
(1)写出SiHCl3的结构式 .
(2)SiHCl3 , 在NaOH溶液中剧烈反应放出H2 , 该反应的化学方程式为 .
(3)硅的平衡转化率与投料比 ![]() 的关系如图,则图中温度T1、T2、T3的大小顺序为 .
的关系如图,则图中温度T1、T2、T3的大小顺序为 . 
(4)平衡时, ![]() 的值a随着
的值a随着 ![]() 的值b的变化而变化.则
的值b的变化而变化.则 ![]() =(用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度. 请用平衡移动原理加以解释 .
=(用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度. 请用平衡移动原理加以解释 .
(5)也可用H2还原SiCl4来制取SiHCl3 . 300℃时该反应的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下四种有机物的分子式皆为C4H10O: 
(1)其中能被氧化成含有相同碳原子数的醛的是(填序号,下同);
(2)能发生消去反应生成两种产物的是;
(3)能被氧化成酮的是;该催化氧化反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前“低碳减排”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂表面积(S)和时间(I)的变化曲线如图所示.据此判断:
①该反应的△H0(填“>”或“<”).
②在T2温度下,0﹣2s内的平均反应速率v(N2)=mol/(Ls).
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号).
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
例如:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)═N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4(g)催化还原N2O4(g)的热化学方程式: .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2(g)和H2O(g)为原料制备HCOOH和O2的原理示意图.催化剂b表面发生的电极反应为 . 
③常温下0.1molL﹣1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=molL﹣1(填写最终计算结果).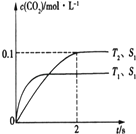
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中含有共价键的离子化合物是( )
①MgF2 ②Na2O2 ③KOH ④CO2 ⑤NaClO ⑥H2SO4 ⑦NH3·H2O
A. ②③⑤B. ②③④⑤C. ①②③⑤D. ①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是( ) 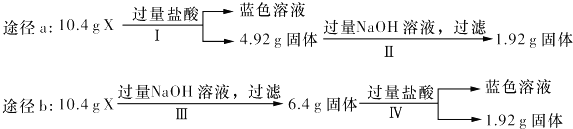
A.由工可知X中一定存在Fe2O3、Cu
B.无法判断混合物中是否含有Al2O3
C.1.92 g固体成分为Cu
D.原混合物中m( Fe2O3):m(Cu)=1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com