
【题目】(一)某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
实验 序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(1)写出草酸与高锰酸钾反应的离子方程式____________。
(2)通过实验A、B,可探究出________(填外部因素)的改变对化学反应速率的影响,其中V1=_______、T1=______/span>;通过实验______(填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_____。
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=____mol·L-1·min-1。
(二)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2):

(1)上表试管Ⅰ中应添加的试剂为5滴____________。
(2)结论是_________,实验Ⅲ的目的是__________。
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 浓度 1 293 BC 3 0.05mol·L-1· min-1 0.1 mol·L-1 FeCl3溶液 Fe3+和Cu2+对H2O2的分解均有催化作用,且Fe3+比Cu2+催化效果好 对比实验,证明Cl-对H2O2的分解没有催化作用
【解析】
(一) (1)KMnO4与草酸在酸性条件发生氧化还原反应,产生Mn2+、CO2、H2O,根据电子守恒、电荷守恒及原子守恒,书写反应的离子方程式;
(2)A、B应控制温度相同,探究浓度对反应速率的影响,B、C温度不同可探究温度对反应速率的影响,研究某种因素对反应速率的影响时,需要保证气体条件相同;
(3)结合v=![]() 计算z反应速率;
计算z反应速率;
(二)要对比Fe3+和Cu2+对H2O2分解反应的催化效果,试管II是CuCl2,则试管I应该为FeCl3溶液,还必须排除溶液中的阴离子是否有催化作用,试管Ⅲ就很好的解决了这个问题。
(一) (1)KMnO4与草酸在酸性条件发生氧化还原反应,产生Mn2+、CO2、H2O,根据电子守恒、电荷守恒及原子守恒,可得该反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)实验A、B,滴加H2C2O4溶液的体积不等,故实验A、B可探究出H2C2O4浓度的改变对反应速率的影响;据实验A可知,保证溶液的总体积为6mL,B中H2C2O4溶液3mL,故需加水的体积V(H2O)=6mL-2mL-3mL=1mL;
A、B研究浓度对化学反应速率的影响,需要温度相同,故T1=293;
B、C温度不同,要探究出温度变化对化学反应速率的影响,其余条件相同,则V2=6mL-2mL-1mL=3mL;
(3)根据实验B中数据可知,高锰酸钾完全反应需要的时间为8s,高锰酸钾的物质的量n(KMnO4)=0.02mol/L×0.002L=0.00004mol,混合后溶液中高锰酸钾的浓度c(KMnO4)=![]() =
=![]() ×10-3mol/L,则用KMnO4的浓度变化表示的反应速率v(KMnO4)=
×10-3mol/L,则用KMnO4的浓度变化表示的反应速率v(KMnO4)= =8.3×10-4mol/(Ls)= 0.05mol/(L· min);
=8.3×10-4mol/(Ls)= 0.05mol/(L· min);
(二)试管Ⅰ、试管Ⅱ是为验证Fe3+和Cu2+对H2O2分解反应的催化效果,所用试剂的浓度、用量要完全一样,试管Ⅱ是是CuCl2,则试管I应该为FeCl3溶液,是5滴FeCl3溶液,试管Ⅲ无气泡产生,试管Ⅲ是一个对比实验,说明Cl-对H2O2的分解没有催化作用,试管I产生气泡快,多,试管II产生的气泡少,慢,从而得到Fe3+和Cu2+对H2O2的分解均有催化作用,且Fe3+比Cu2+催化效果好的结论,证明Cl-对H2O2的分解没有催化作用。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)![]() 4C(s)+D(g),2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是
4C(s)+D(g),2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是
A.前2 min,D的平均反应速率为0.2 mol/(L·min)
B.B的平衡转化率是40%
C.增大该体系的压强,平衡不移动
D.增加B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铁盐与亚硫酸盐之间的反应,某研究小组利用孔穴板进行了实验探究:
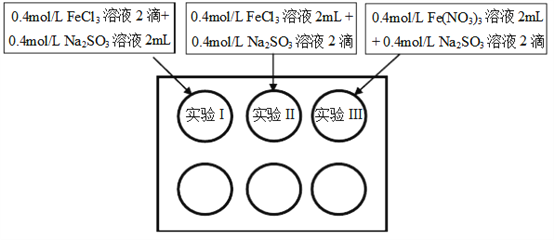
小组记录的实验现象如下表所示:
开始时 | 5min后 | 3天后 | |
实验I | 溶液立即变为红褐色,比II、III中略浅 | 与开始混合时一致 | 溶液呈黄色,底部出现红褐色沉淀 |
实验II | 溶液立即变为红褐色 | 红褐色明显变浅 | 溶液呈黄绿色 |
实验III | 溶液立即变为红褐色 | 红褐色变浅,比II中深 | 溶液呈黄色 |
(1)测得实验所用0.4mol/L FeCl3溶液及Fe(NO3)3溶液pH均约为1.0。两溶液均呈酸性的原因是__________(用离子方程式表示)。
(2)开始混合时,实验I中红褐色比II、III中略浅的原因是___________。
(3)为了探究5min后实验II、III中溶液红褐色变浅的原因,小组同学设计了实验IV:分别取少量5min后实验I、II、III中溶液,加入2滴铁氰化钾溶液,发现实验II、III中出现蓝色沉淀,实验I中无明显变化。根据实验IV的现象,结合化学用语解释红褐色变浅的原因是___________。
(4)针对5min后实验III中溶液颜色比实验II中深,小组同学认为可能存在三种因素:
①Cl- 可以加快Fe3+与SO32-的氧化还原反应;
②___________;
③NO3- 在酸性环境下代替Fe3+氧化了SO32-,同时消耗H+,使Fe3+水解出的Fe(OH)3较多。
通过实验V和实验VI进行因素探究:
实验操作(已知Na+对实验无影响) | 5min后的现象 | |
实验V | 在2mL pH=1.0的0.4mol/L Fe(NO3)3溶液中溶解约___________固体,再加入2滴0.4mol/L Na2SO3溶液 | 溶液的红褐色介于II、III之间 |
实验VI | 在2mL pH=1.0的稀硝酸中溶解约0.19g NaNO3固体,再加入2滴0.4mol/L Na2SO3溶液。向其中滴入少量BaCl2溶液 | _____________ |
实验结论:因素①和因素②均成立,因素③不明显。请将上述方案填写完整。
(5)通过上述实验,以下结果或推论合理的是___________(填字母)。
a.Fe3+与SO32-同时发生水解反应和氧化还原反应,且水解反应的速率快,等待足够长时间后,将以氧化还原反应为主
b.浓度为1.2 mol/L的稀硝酸在5min内不能将Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用来检验实验I的上层清液中是否存在SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84g·cm-3)配制1mol·L-1的稀硫酸100 mL,现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒。按实验时使用仪器的先后顺序,排列正确的是 ( )
A.②⑥③⑦⑤⑥B.②③⑦⑤⑥C.①③⑤⑦④⑥D.④⑦③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 某无色溶液中可能含有
某无色溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种,依次进行下列实验。观察到现象如下:
中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液![]() ;
;
②向溶液中滴加氯水,无气体产生,再加入![]() 振荡、静置,
振荡、静置,![]() 层呈橙红色,用分液漏斗分液;
层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入![]() 和
和![]() 混合液,有白色沉淀产生。
混合液,有白色沉淀产生。
④另取原溶液少量加入![]() 和盐酸的混合液,产生白色沉淀。
和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是_________;肯定没有的离子是_________。
(2)写出步骤②中的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1) 配制待测液:称取6.0 g固体烧碱样品(杂质不与酸反应)配制成250 mL溶液。
(2) 滴定:
①用_______量取15.00 ml.待测液。
②向锥形瓶中加入几滴甲基橙,用0.2010 mol L-1的标准硫酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,滴定终点时的现象为________________。
(3)数据处理
实验次 序编号 | 硫酸溶液体积 V/mL | 氢氧化钠溶液体积 V/mL |
1 | 19.90 | 15.00 |
2 | 20.10 | 15.00 |
3 | 22.00 | 15.00 |
4 | 20.00 | 15.00 |
根据上述表格,选取合适的数据,计算待测烧碱溶液的浓度为______________,碱的纯度为_______________(保留两位小数)。
(4)—定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制盐酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是
__________________(多选)
A.实验中所用到的滴定管、容量瓶,在使用前均需要验漏
B.如果实验中需用80 mL的稀盐酸标准溶液,配制时应选用100mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀盐酸,则测得的NaOH溶液的浓度将偏小
E.配制标准溶液时,定容时俯视读数,则导致滴定时测得的NaOH溶液的浓度偏大
F.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏小
G.锥形瓶用蒸馏水洗浄后,有少量蒸馏水残留,则导致实验结果偏小
H.滴定前滴定管尖嘴有气泡,滴定后气泡消失,则导致实验结果偏大
I.在滴定过程中,不慎将数滴酸液滴在锥形瓶外,则导致实验结果偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中正确的是( )
A. 制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛
B. 炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
C. 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D. 炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.1mol·L-1、体积为V0的HX、HY溶液,分别加水稀释至体积V,pH随lg ![]() 的变化关系如图所示。下列叙述正确的是( )
的变化关系如图所示。下列叙述正确的是( )
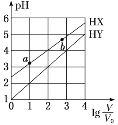
A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.常温下,由水电离出的c(H+)·c(OH-):a<b
C.相同温度下,电离常数K(HX):a>b
D.lg ![]() =3,若同时微热两种溶液,则
=3,若同时微热两种溶液,则![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出![]() 中官能团的名称为_________________;
中官能团的名称为_________________;
(2)![]() 的分子式为_____________,1 mol该有机物完全燃烧需消耗氧气的物质的量为________mol,分子中一定共面的原子有________个;
的分子式为_____________,1 mol该有机物完全燃烧需消耗氧气的物质的量为________mol,分子中一定共面的原子有________个;
(3)有机物M(![]() )为苯的同分异构体,M的二氯代物的同分异构体有____种;
)为苯的同分异构体,M的二氯代物的同分异构体有____种;
(4)用系统命名法对下列有机物进行命名:
① CH3C(CH3)=CHCH3:______________;
② CH3CH(CH2CH3)CH(CH3)CH2CH3:_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com