
当铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率增大的是()
A. 不用稀硫酸,改用98%的浓硫酸
B. 加热
C. 适当增大稀硫酸的浓度
D. 不用铁片,改用铁粉
考点: 化学反应速率的影响因素.
分析: 增大反应速率的方法有:增大反应物浓度、升高温度、增大压强(仅对有气体参加的反应)、加入催化剂、增大反应物的接触面积等,据此分析解答.
解答: 解:A.浓硫酸和铁发生钝化现象,且浓硫酸和铁反应生成二氧化硫而不是氢气,故A选;
B.升高温度,增大活化分子百分数,所以反应速率加快,故B不选;
C.适当增大稀硫酸浓度,增大单位体积内氢离子浓度,反应速率加快,故C不选;
D.不用铁片,改用铁粉,增大反应物接触面积,加快反应速率,故D不选;
故选A.
点评: 本题考查化学反应速率影响因素,明确影响化学反应速率的原理是解本题关键,知道各个条件的适用范围,易错选项是A.


科目:高中化学 来源: 题型:
下列装置所示的实验中,能达到实验目的的是( )
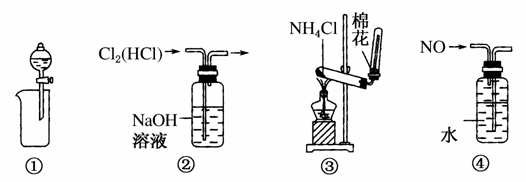
A.①从Mg(OH)2悬浊液中分离出Mg(OH)2
B.②除去Cl2中的HCl
C.③实验室制氨气
D.④排水法收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、HCO3﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()
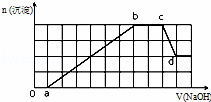
A. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B. ab段发生的离子反应为:Al3++3OH﹣=Al(OH)3↓,Mg2++2OH﹣=Mg(OH)2↓
C. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D. d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素原子最外层上只有两个电子,该元素()
A. 一定是金属元素
B. 一定是ⅡA族元素
C. 一定是过渡元素
D. 可能是金属元素,也可能不是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y均为1~18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则这两种元素的原子序数之和为()
A. 19 B. 18 C. 16 D. 9
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中前者属于取代反应,后者属于加成反应的是()
A. 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液退色
B. 苯与硝酸在一定条件下反应生成硝基苯;乙烯与溴的四氯化碳溶液反应
C. 乙烯与水生成乙醇的反应
D. 在苯中滴入溴水,水层褪色;乙烯与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.向Mg(HCO2)3溶液中滴加过量的NaOH溶液的离子方程式:Mg2++2HCO3﹣+2OH﹣═MgCO3↓+CO32﹣+2H2O
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42﹣完全沉淀的离子方程式:2Ba2++NH4++Al3++2SO42﹣+4OH﹣═Al(OH)3↓+NH3·H2O+2BaSO4↓
C.用稀醋酸除去铜绿的离子方程式:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O
D.已知:
| 共价键 | C﹣C | C=C | C﹣H | H﹣H |
| 键能/kJ·mol﹣1 | 348 | 610 | 413 | 436 |
则可以计算出反应 的△H为﹣384 kJ·mol﹣1
的△H为﹣384 kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,能在溶液中大量共存的是( )
|
| A. | H+、Na+、CO32﹣、Cl﹣ | B. | Ba2+、Na+、Cl﹣、SO42﹣ |
|
| C. | K+、H+、SO42﹣、OH﹣ | D. | Ag+、Al3+、NO3﹣、H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com