
| A. | Na2CO3+H2SO4═CO2↑+H2O+Na2SO4 | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | CO2+2Mg$\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C | D. | CO2+Na2O=Na2CO3 |
分析 能与水作用生成酸或与碱作用生成盐和水的氧化物为酸性氧化物,酸性氧化物与碱性氧化物反应只生成盐,据此解答.
解答 解:A.Na2CO3+H2SO4═CO2↑+H2O+Na2SO4,二氧化碳与水反应生成碳酸,符合酸性氧化物的概念,故A正确;
B.二氧化碳与碱反应只生成盐和水,符合酸性氧化物的概念,故B正确;
C.CO2+2Mg$\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C为氧化还原反应,不能证明二氧化碳为酸性氧化物,故C错误;
D.二氧化碳与碱性氧化物反应只生成盐,符合酸性氧化物的概念,故D正确;
故选:C.
点评 本题考查了酸性氧化物判断,明确酸性氧化物的概念及性质是解题关键,题目难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | CO | B. | NO | C. | CO2 | D. | N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:1 | C. | 1:2 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 molNa2O2与足量的CO2充分反应转移的电子数为0.2NA | |
| B. | 常温常压下,18g H2O 所含的中子数为8NA | |
| C. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移 | |
| D. | 将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、NO3-、CO32- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Na+、Ag+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
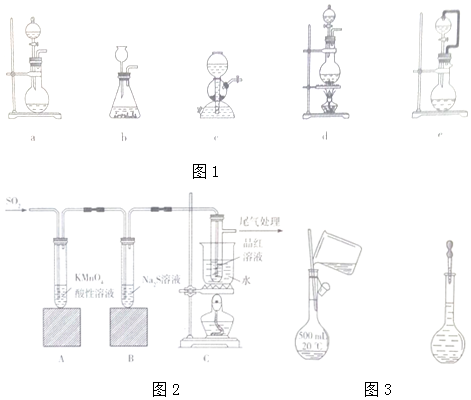
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发现放射性元素钋和镭 | B. | 现代量子化学的创立 | ||
| C. | 人工全合成牛胰岛素 | D. | 元素周期律的发现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 | |
| D. | 101 kPa时,硫的标准燃烧热与硫完全燃烧时的物质的量无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com