
| A. | 可用排水法收集二氧化氮气体 | |
| B. | 浓硝酸存放于棕色广口试剂瓶中 | |
| C. | 配制氯化亚铁溶液时,将氯化亚铁固体溶解在蒸馏水中加少量盐酸即可 | |
| D. | 蒸馏时应先向冷凝管中通入冷凝水再加热 |
分析 A.二氧化氮与水发生化学反应;
B.液体存放在细口瓶;
C.氯化亚铁具有还原性,亚铁离子易水解;
D.若先加热后通冷凝水,蒸汽得不到冷凝,可能造成大气污染.
解答 解:A.二氧化氮与水反应生成硝酸和一氧化氮,因此不能用排水法收集,故A错误;
B.浓硝酸见光易分解,应存放于棕色细口试剂瓶中,故B错误;
C.实验室配制氯化亚铁溶液时,可先将氯化亚铁溶解在盐酸中,再加入蒸馏水稀释,最后加入少量铁屑,故C错误;
D.若先加热后通冷凝水,蒸汽得不到冷凝,产品得不到回收,也可能造成大气污染,故D正确;
故选D.
点评 本题考查化学实验基本操作,涉及药品的保存、气体的收集、溶液的配制以及蒸馏操作的注意事项,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4NO3 | B. | NaOH | C. | MgSO4 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
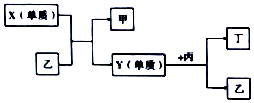 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )| A. | 原子半径的大小:W<Y<Z<X | B. | 单质与H2化合的难易程度:X>Y | ||
| C. | 甲与丙反应不可能生成离子化合物 | D. | Z的最高价氧化物的水化物为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W<X<Y<Z | |
| B. | 简单氢化物的稳定性:X>Y>Z | |
| C. | W分别与X、Z形成的化合物均能抑制水的电离 | |
| D. | 在化合物A 的分解反应中丙为氧化产物,丁为还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CsICl2常用于化学上的分子筛技术,它既有氧化性又有还原性,CsICl2有还原性是因为有较强还原性的I- | |
| B. | “神舟十一号”宇宙飞船成功与“天宫二号”对接,其太阳能光电池材料是硅 | |
| C. | 司母戊鼎、辽宁舰甲板、超轻钨碳塑钢眼镜框架等原材料属合金 | |
| D. | 硅橡胶能耐高温和耐低温是新型的无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
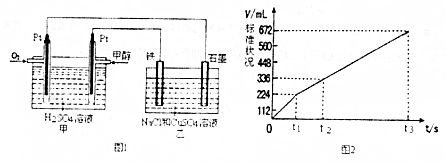
| 容器 | A | B |
| 反应物投入量 | 1molCO2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
| 反应能量变化 | 放出29.4KJ | 吸收aKJ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
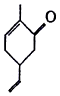
| A. | 可以发生氧化反应 | B. | 分子式为C9H10O | ||
| C. | 分子中所有原子都处于同一平面上 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L的NH4HSO4溶液:Ba2+、Na+、NO3-、Cl- | |
| B. | 通KSCN溶液变红色的溶液:NH4+、Al3+、SO42-、Cl- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1014的溶液:Ca2+、Na+、ClO-、NO3- | |
| D. | 与铝反应产生大量氢气的溶液:K+、Na+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com