
 “摩尔盐”1(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.已知:摩尔盐隔绝空气加热至500℃时可完全分解.某学习小组欲探究其分解产物.
“摩尔盐”1(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.已知:摩尔盐隔绝空气加热至500℃时可完全分解.某学习小组欲探究其分解产物.分析 (1)摩尔盐中N为-3价,Fe为+2价,S为+6价,根据产物中化合价分析;
(2)摩尔盐中含有的三种离子分别为亚铁离子、硫酸根和铵根,验证铵根需要氢氧根、验证硫酸根需要钡离子,依据所给试剂判断还需要氢氧化钡;亚铁离子若变质应生成铁离子,铁离子遇KSCN变红色;
(3)①A中固体充分加热较长时间后,通入氮气目的是使分解生成的气体在BC装置中完全吸收;
②C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4;
③高锰酸钾具有氧化性,亚铁离子具有还原性,高锰酸钾溶液不褪色,说明不含有亚铁离子;
(4)分析(3)中实验②③得出,分解产物中一定含有SO2,一定不含有FeO,据此解答即可.
解答 解:(1)摩尔盐中N为-3价,Fe为+2价,S为+6价,
A.Fe2O3、SO2、NH3、H2O 反应时Fe元素的化合价升高,S元素化合价降低,符合氧化还原反应规律,故A正确;
B.FeO、NH3、SO3、H2O,反应时没有元素化合价的变化,只是发生分解反应,故B正确;
C.FeO、SO2、NH3、H2O反应时只有S元素的化合价降低,不符合氧化还原反应规律,故C错误;
D.Fe2O3、NH3、SO2、SO3、H2O反应时,Fe的化合价升高,S的化合价降低,符合氧化还原反应规律,故D正确,
故答案为:C;
(2)摩尔盐中含有的三种离子分别为亚铁离子、硫酸根和铵根,验证铵根需要氢氧根、验证硫酸根需要钡离子,依据所给试剂判断还需要氢氧化钡;亚铁离子若变质应生成铁离子,铁离子遇KSCN变红色,若不变红色,说明未被氧化,
故答案为:Ba(OH)2;硫氰化钾溶液,溶液不变红色;
(3)①A中固体充分加热较长时间后,产生气体有一部分残留在装置中,通入氮气可以使分解生成的气体在B、C装置中完全吸收,
故答案为:使分解产生的气体在B、C中被吸收充分;
②C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4则C中发生的反应为SO2+H2O2+Ba2+=BaSO4↓+2H+,
故答案为:SO2+H2O2+Ba2+=BaSO4↓+2H+;
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含有还原性的物质,即不含有FeO,
故答案为:FeO;
(4)根据上述分析知,“摩尔盐”分解的产物为Fe2O3、SO3、SO2、NH3 和H2O,上述猜想中一定正确的是D,故选D,
故答案为:D.
点评 本题考查了物质性质的实验探究和实验设计,题目涉及氧化还原反应、离子方程式的书写、离子检验、实验基本操作等,侧重于考查学生对基础知识的综合应用能力,题目难度中等.


科目:高中化学 来源: 题型:解答题
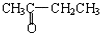 B.
B.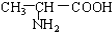 与
与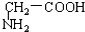
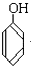 与
与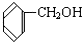 D.CH3CH2C≡CH与CH2═CH-CH═CH2E.
D.CH3CH2C≡CH与CH2═CH-CH═CH2E.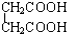 与
与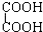 F.戊烯和环丙烯
F.戊烯和环丙烯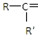 氧化成(R、R′
氧化成(R、R′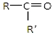 可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 种 | B. | 16 种 | C. | 18 种 | D. | 19 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1 mol•L-1的氨水中含有0.1NA个OH- | |
| B. | 78gNa2O2固体中含有的阴离子数目为2NA | |
| C. | 常温下,23gNO2和N2O4的混合气体含有NA个氧原子 | |
| D. | 常温下,4gCH4中含有4NA个C-H共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
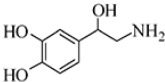
| A. | 每个去甲肾上腺素分子中含有2个酚羟基 | |
| B. | 去甲肾上腺素能与酸性KMnO4溶液反应 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ③①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.00 mol•L-1 | B. | 0.500 mol•L-1 | C. | 2.00 mol•L-1 | D. | 3.00 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com