
�ռ����ȶ�����Ҫ�Ļ���ԭ�ϡ�
(1)������ͼװ�ÿ���֤��������̼���ռ���Һ�����˷�Ӧ��
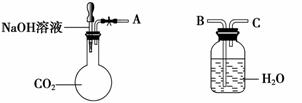
������A��B���ӣ���ֹˮ�У�����ͷ�ι��е�Һ�強����ƿ����ʱ��ʵ��������______
_____________________________________________________________��
���������������䣬��A��C���ӣ��ɹ۲쵽��������_____________________��
(2)��100 mL 1 mol·L��1�ռ���Һ��ͨ��һ����CO2��ַ�Ӧ����Һ�ڵ��������ɵõ���ɫ����X��X����ɿ�������������������ֵ��Ⱥ�˳��ֱ��Ǣ�.NaOH��Na2CO3����.__________________����.Na2CO3��NaHCO3����.__________________��
�ٳ����£����õ��Ĺ���X��������ˮ����������Һ����μ������ᣬ�õ�����ı仯ͼ����X�ijɷ�Ϊ (�����)�������Ũ��Ϊ ��
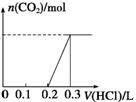
����Ҫ��֤��ɫ����X�ǵڢ�����ɣ�����������Լ�Ϊ________(����ĸ���)��
a������ b��MgCl2��Һ c��BaCl2��Һ d��Ba(OH)2��Һ
����֤�Ĺ����У�һ����Ҫ���еIJ�����________(����ĸ���)��
a����ȡ b��ϴ�� c������ d������
������ɫ����XΪ�ڢ�����ɣ�����ʵ�鷽���в��ܲⶨ����NaHCO3������������________(����ĸ���)��
a��ȡm g X������Ba(OH)2��Һ��ַ�Ӧ�����ˣ�ϴ�ӣ���ɵ�n g����
b��ȡm g X�����������ַ�Ӧ�����ȣ����ɣ����յ�n g����
c��ȡm g X��ּ��ȣ�����n g
d��ȡm g X������ϡ�����ַ�Ӧ���ݳ������屻������ʯ�����գ�����n g
������ɫ����X������Ϊ5.0 g����X�����Ϊ________(�����)��
��֪ʶ�㡿Ԫ�ػ��������A1 C5
���𰸽�����(1)��ˮ�ص����ɹ��ƿ������ƿ �ڹ��ƿ�еij����ܿ������ݲ���
(2)Na2CO3��NaHCO3 ��I��0.33mol/L����cb��˳���ܷ�����c����d����I
��ÿ��1�֣�
������ �Ţٽ�A��B���ӣ���ֹˮ�У�����ͷ�ι��е�Һ�強����ƿ���������̼���ռ���Һ�����˷�Ӧ������ѹǿ��С������ˮ�ص����ɹ��ƿ������ƿ��
���������������䣬����A��C���ӣ�ͬ����������������뼯��ƿ���ɹ۲쵽�������ǹ��ƿ�еij����ܿ������ݲ�����
������CO2��NaOH��Ӧʱ���ʵ���֮�Ȳ�ͬ����ﲻͬ���ʿɸ���CO2��NaOH��Ӧʱ���ʵ���֮�ȶԲ���������ۣ���n��NaOH����n��CO2��>2:1ʱ��XΪNaOH��Na2CO3�Ļ���n��NaOH����n��CO2��=2:1ʱ��XΪNa2CO3��1<n��NaOH����n��CO2��<2:1ʱ��XΪNaHCO3��Na2CO3�Ļ���n��NaOH����n��CO2����1:1ʱ��XΪNaHCO3����Na2CO3��HCl��Ӧ���£�Na2CO3+HCl=NaCl+ NaHCO3��NaHCO3+HCl=NaCl+H2O+ CO2�����ͼ֪����������ᣬһ��ʼû���������������ǰ�����ĵ����ᣨ0.2L���Ⱥ�����ĵ����ᣨ0.1L���࣬�������NaOH��Na2CO3�Ļ����������Ȼ�������̼���Ʋ���ȥ̼���ƣ�Ȼ�����Ȼ�þ�����������ƣ���֤��������Ҫ�ѳ������˺��ټ������������ӣ����漰�IJ����ǹ��ˢ�����ɫ����XΪ�ڢ�����ɣ�Na2CO3��NaHCO3 ��a������������̼�����Ʒ�Ӧ����̼�ᱵ��������̼���Ʒ�Ӧ����̼�ᱵ����������̼���ƺ�̼�����ƻ��������Ϊm������̼�ᱵ��������Ϊng������̼Ԫ���غ���ʽ����NaHCO3����������b��ȡmg X�����������ַ�Ӧ�����ȣ����ɣ����յ�n g����Ϊ�Ȼ��ƣ�������Ԫ�� �غ���ʽ���㣬����NaHCO3����������c��ȡm g X��ּ��ȣ�����n g�������ķ�Ӧ��̼���������ȷֽ⣬������������Ϊˮ�Ͷ�����̼�����ͽ�ϻ�ѧ����ʽ����õ�̼����������������NaHCO3����������d��ȡm g X������ϡ�����ַ�Ӧ���ݳ��������Ƕ�����̼��ˮ��������������ʯ�����գ�����n g����������̼��ˮ����������Ϊng���������������̼��ˮ�������������٣��������㲻��̼�����Ƶ�������������ѡd��
��100mL 1mol•L-1�ռ���Һ�к��������������ʵ���Ϊ0.1mol��������Ԫ���غ���ȫ������Na2CO3����������=0.05��106=5.3g�����������Ʋ��μӷ�Ӧ������������4g��5.0g���ڶ���֮�䣬�����NaOH��Na2CO3�Ļ���
��˼·�㲦���漰�ۺϼ���ʱ�������غ㷨��ԭ���غ㡢����غ㡢��ʧ�����غ㣻�������䷨�������������������̼��Ӧ�IJ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о�С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
��1�������SO2�����NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��
SO2��2NaOH===������������������
��2����ӦCl2��Na2SO3��2NaOH===2NaCl��Na2SO4��H2O�еĻ�ԭ��Ϊ����������
��3������β��һ��ʱ�������Һ��ǿ���ԣ��п϶�����Cl����OH����SO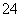 �������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
������������衣
����1��ֻ����SO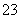 ������2���Ȳ�����SO
������2���Ȳ�����SO ��Ҳ������ClO��������3��������������������������
��Ҳ������ClO��������3��������������������������
�����ʵ�鷽��������ʵ�顣��д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ���ѡʵ���Լ���3 mol·L��1 H2SO4��1 mol·L��1NaOH��0.01 mol·L��1KMnO4�����ۣ�KI��Һ����ɫʯ����Һ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ�������£����ڿ��淴ӦX(g)��3Y(g) 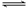 2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3(����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol·L-1��0.3mol·L-1��0.08 mol·L-1���������ж���ȷ����
2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3(����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol·L-1��0.3mol·L-1��0.08 mol·L-1���������ж���ȷ����
A��c1��c2��3��1
B��X��Y��ת���ʲ����
C��ƽ��ʱ��Y��Z����������֮��Ϊ2��3
D��c1��ȡֵ��ΧΪ0 mol·L-1<c1<0.14 mol·L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ����٤������������˵����ȷ���ǣ� ��
A.��״���£�11.2L��ϩ���еļ��Թ��ۼ���ΪNA
B.�����£�5.6LNO��5.6LO2�Ļ�������к��еķ�����Ϊ0.5NA
C.16.9gBaO2��������������������Ϊ0.2NA
D.����1molFe(OH)3���������������к��н�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ����٤����������ֵ������˵����ȷ����
A. 0.1 mol·L-1��NaF��Һ������F-����ĿС��0.1NA
B. ��״���£�2.24L�Ҵ��к��е�C—H����ĿΪ0.5NA
C. 0.1 molNa��ȫ����������Na2O2��ת�Ƶ��ӵ���ĿΪ0.1NA
D. 0.1 molO3�к���ԭ����ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ײ�����ȱλ������(MFe2Ox��3<x<4��M=Mn��Zn��Ni�Ҿ���+2������ͬ)��������(MFe2O4)�����»�ԭ���á������£�����ʹ��ҵ�����е�����������ֽ��ȥ��ת��������ͼ��ʾ��

(1)��֪������(MFe2O4)��H2���»�ԭʱ��������Ӧ��MFe2O4��H2�����ʵ���֮��Ϊ 2︰1����ԭ���� MFe2Ox ��x=______��MFe2Ox ��+2������+3��������֮��Ϊ_____��
(2)��������Һ����Fe2O42����ת��ΪFe2��:Fe2O42����2e����8H����2Fe2����4H2O�� KMnO4��Na2CO3��Cu2O��Fe2(SO4)3 ���������е�һ����ʹ������ԭ���̷�����д����������ԭ��Ӧ�����ӷ���ʽ����ƽ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��A�����������(Se)����(Te)��Ԫ���ڻ������г����ֳ���������̬������A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⡣
(1)S���ʵij�����ʽΪS8���价״�ṹ��ͼ��ʾ��Sԭ�Ӳ��õĹ���ӻ���ʽ��________��
(2)ԭ�ӵĵ�һ��������ָ��̬�����Ի�̬ԭ��ʧȥһ������ת��Ϊ��̬��̬����������Ҫ�����������O��S��Seԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ________��
(3)Seԭ������Ϊ____________�������M����ӵ��Ų�ʽΪ________��
(4)H2Se�����Ա�H2S________(�ǿ��������)����̬SeO3���ӵ����幹��Ϊ__________��SO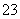 �����幹��Ϊ________��
�����幹��Ϊ________��
(5)H2SeO3��K1��K2�ֱ�Ϊ2.7��10��3��2.5��10��8��H2SeO4��һ��������ȫ���룬K2Ϊ1.2��10��2������ݽṹ�����ʵĹ�ϵ���ͣ�
��H2SeO3��H2SeO4��һ������̶ȴ��ڵڶ��������ԭ��________________________________________��
��H2SeO4��H2SeO3����ǿ��ԭ��__________________________ ______________��
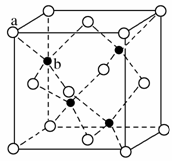
(6)ZnS��ӫ���塢�����ϡ�Ϳ�ϡ����ϵ���ҵ��Ӧ�ù㷺������ZnS����ṹ��ͼ��ʾ���侧���߳�Ϊ540.0 pm���ܶ�Ϊ______g·cm��3(��ʽ������)��aλ��S2����bλ��Zn2��֮��ľ���Ϊ______pm(��ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ�����������˵����ȷ���ǣ� ��
A. 1L 0.1mol/L��Na2CO3��Һ�У���Na+0.2 NA����CO32-0.1 NA��
B. 1L 0.3mol/L��K2SO4��Һ�У���K+��SO42-��������Ϊ0.9 NA��
C. 2L 0.6mol/L��Fe2��SO4��3��Һ�У���SO42-��������Ϊ2.4 NA��
D. 0.1mol/L��H3PO4��Һ�У�c(H+)��c(PO43-)<3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���д������ (����)
A����1 L 1 mol/L��NaCl��Һ��ȡ��10 mL����Ũ������1 mol/L
B���Ƴ�0.5 L 10 mol/L�����ᣬ��Ҫ�Ȼ�������112 L(��״��)
C��0.5 L 2 mol/L BaCl2��Һ�У�Ba2����Cl������Ϊ3��6.02��1023
D��10 g 98%������(�ܶ�Ϊ1.84 g/cm3)��10 mL 18.4 mol/L�����Ũ���Dz�ͬ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com