
下列有关电子排布图的表述正确的是( )
A. 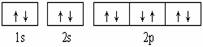 可表示单核10电子粒子基态时电子排布
可表示单核10电子粒子基态时电子排布
B. 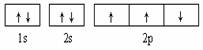 此图错误,违背了泡利原理
此图错误,违背了泡利原理
C.  表示基态N原子的价电子排布
表示基态N原子的价电子排布
D. 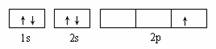 表示处于激发态的B的电子排布图
表示处于激发态的B的电子排布图
科目:高中化学 来源: 题型:
交警对驾驶员是否饮酒进行检测的原理是橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是 ( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇具有还原性
④乙醇是烃的含氧衍生物 ⑤乙醇可与羧酸在浓硫酸的作用下发生取代反应
A.②⑤ B.②③
C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A.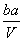 mol·L-1 B.
mol·L-1 B. mol·L-1
mol·L-1
C.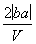 mol·L-1 D.
mol·L-1 D.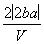 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液配制实验的描述完全正确的是( )
A.在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
B.用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1)通常需要用容量瓶等仪器
C.配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解
D.用pH=1的盐酸配制100 mL pH=2的盐酸所需全部玻璃仪器有100 mL容量瓶、烧杯、玻璃棒、胶头滴管
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
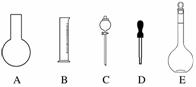
(1)如图所示的仪器中配制溶液肯定不需要的是
(填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
(2)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为 g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度 (填“>”、“<”或“=”)0.1 mol·L-1;
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度 (填“>”、“<”或“=”)0.1 mol·L-1。
(3)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为 (计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL量筒,应选用 mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于乙烯分子中的共价键,下列描述正确的是( )
A.含有5个σ键、1个π键
B.C-H之间是碳的sp2杂化轨道与H的s轨道形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键
C.只有sp2杂化轨道才形成π键
D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质,以CH4为燃料时,该电池工作原理如下图所示。下列说法正确的是( )
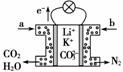
A.a为CH4,b为CO2
B.CO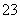 向正极移动
向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为O2+2CO2+4e-===2CO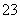
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,体积一定的密闭容器中进行如下可逆反应:
X(g)+Y(g) Z(g)+W(s)ΔH>0下列叙述正确的是( )
Z(g)+W(s)ΔH>0下列叙述正确的是( )
A.当容器中气体压强不变时,反应达到平衡
B.升高温度,平衡逆向移动
C.加入少量W,逆反应速率增大
D.平衡后加入X,上述反应的ΔH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com