
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | Cl-、Cl为不同的核素,有不同的化学性质 | |
| C. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| D. | 电解饱和食盐水制氯气时,与电源负极相连的石墨棒上方充满黄绿色气体 |
分析 A.氯气既具有氧化性,也具有还原性;
B.根据核素的定义判断;
C.氯气不溶于饱和食盐水;
D.电解饱和食盐水制氯气时,与电源负极相连的石墨棒上生成氢气.
解答 解:A.氯气既具有氧化性,也具有还原性,如水、氢氧化钠等反应时,氯气既具有氧化性也表现了还原性,故A错误;
B.如中子数相同,则为同一核素,但核素只原子,而Cl-为离子,故B错误;
C.氯气不溶于饱和食盐水,可用排饱和食盐水集气法收集,故C正确;
D.电解饱和食盐水制氯气时,与电源负极相连的石墨棒上生成氢气,氯气在阳极生成,故D错误.
故选C.
点评 本题考查物质的性质,为高频考点,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,注意把握氯气的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
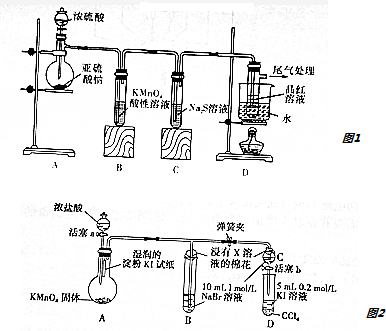
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| a | |||||||
| b | c | d | |||||
| e | f | g |
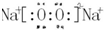 ;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”)
;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
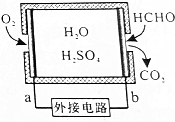
| A. | b为电池负极,甲醛被氧化 | |
| B. | a极的电极反应为O2+4e-+4H+=2H2O | |
| C. | 传感器工作过程中,电解质溶液中硫酸的浓度不变 | |
| D. | 当电路中转移1×10-4mol电子时,传感器内参加反应的HCHO为0.75mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 硝酸银溶液与盐酸反应:Ag++Cl-═AgCl↓ | |
| D. | 澄清石灰水与碳酸钠溶液反应:Ca(OH)2+CO32-═CaCO3↓+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
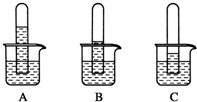
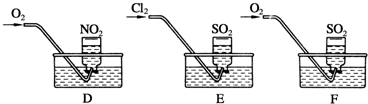
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入二氧化碳气体 | D. | 向水中加醋酸钠晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
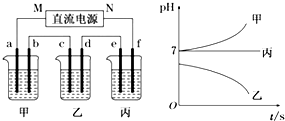
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com