


科目:高中化学 来源: 题型:
| A、只有①②③ | B、①②③④ |
| C、只有①③④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH | 离子浓度关系 | |
| A | pH<7 | c(CH3COO?)>c(Na+) |
| B | pH>7 | c(CH3COO?)<c(Na+) |
| C | pH=7 | c(CH3COO?)=c(Na+) |
| D | pH<7 | c(CH3COO?)<c(Na+) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
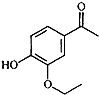 乙基香兰素是一种重要的合成香料,其分子结构如图1所示.从结构推测,乙基香兰素不具有的化学性质是( )
乙基香兰素是一种重要的合成香料,其分子结构如图1所示.从结构推测,乙基香兰素不具有的化学性质是( )| A、与溴水发生取代反应 |
| B、与烧碱溶液反应 |
| C、与NaHCO3溶液反应放出CO2 |
| D、与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol?L-1) | V/mL | c/(mol?L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3O4是一种红棕色粉末,俗称磁性氧化铁 |
| B、铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
| C、去除FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤 |
| D、Fe3+与KSCN反应产生红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯分子呈平面正六边形,六个碳碳键完全相同,键角皆为120° |
| B、苯分子中的碳原子采取sp2杂化,6个碳原子中未参与杂化的2p轨道以“肩并肩”形式形成一个大π键 |
| C、苯分子中的碳碳键是介于单键和双键之间的一种特殊类型的键 |
| D、苯能使溴水褪色,是因为苯将Br2还原为Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com