
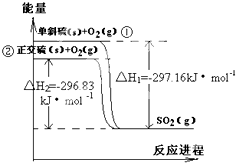
 单斜硫和正交硫转化为二氧化硫的 能量变化图如图,回答下列问题:
单斜硫和正交硫转化为二氧化硫的 能量变化图如图,回答下列问题:

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在任何温度下都能自发进行 |
| B、在任何温度下都不能自发进行 |
| C、仅在高温下自发进行 |
| D、仅在低温下自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应中的能量变化都表现为热量变化 |
| B、△H的大小与热化学方程式的计量数无关 |
| C、生成物的总焓大于反应物的总焓时,反应吸热,△H>0 |
| D、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、微粒半径:O2-<F-<Na+<K+ |
| B、共价键的键能:C-C>C-Si>Si-Si |
| C、分子中的键角:CH4>H2O>CO2 |
| D、共价键的键长:H-F>H-C1>H-Br>H-I |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com