
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl﹣)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂.等物质的量的上述物质消毒效率最高的是 (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称.如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2═A+NH3↑,则生成物A的化学式为 ,H2O2被称为“绿色氧化剂”的理由是 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年.亚氯酸不稳定可分解,反应的离子方程式为HClO2 → ClO2↑+H++Cl﹣+H2O(未配平)。在该反应中,当有1mol ClO2生成时转移的电子个数约为 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是 (用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式 。
科目:高中化学 来源:2016届甘肃省天水市高三上学期第三次测试化学试卷(解析版) 题型:推断题
以下均为中学化学常见物质,存在如下转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
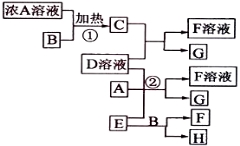
(1)G的化学式 ;F的电子式 ;
(2)反应①的离子方程式 ;
(3)写出另外一种实验室制取H的化学方程式 ;
(4)D溶液中阳离子的焰色反应火焰呈 色;可用 试剂检验D溶液中大量存在的阴离子。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高一10月月考化学试卷(解析版) 题型:计算题
将BaCl2·xH2O的晶体2.44克溶于水配成100mL溶液,取此溶液25mL与50mL0.1mol/L的AgNO3溶液作用,刚好把Cl-离子沉淀完全。①求2.44克的BaCl2·xH2O的物质的量。
②求BaCl2·xH2O的摩尔质量。③求BaCl2·xH2O的晶体的x的值。
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期10月阶段性教学质检化学试卷(解析版) 题型:选择题
粒子甲在溶液中的转化关系如下图所示,粒子甲不可能是

A.NH4 + B.Al(OH)3 C.S D.Al
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:推断题
A、B、C、D均为中学化学所学的常见物质,它们之间的转化关系如下列各图所示(部分反应条件或产物已略去).请按要求回答下列问题:
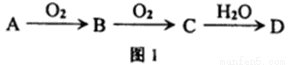
(1)若A、B、C、D均含有同一种短周期元素X,它们的转化关系如图l所示:
①常温下,若A为化合物,C为红棕色气体,D为强电解质,则X所在周期表中的位置是 ;用方程式表示A溶于水,使酚酞变红的原因: .
②常温下,若A为固体单质,D为强电解质,则D可能的化学式为 、 .符合上述条件且含有离子键的C的电子式: .
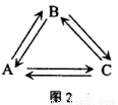
(2)若A、B、C均含有同一种短周期元素Y,它们的转化关系如图2所示:
若Y的周期数等于主族序数;盐A溶液显酸性:盐B溶液显碱性,且焰色反应为黄色;C为两性氢氧化物。请用离子方程表示B溶液显碱性的原因: ;在实验室里,欲使A溶液中的阳离子全部沉淀出来转化为C,所发生化学反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源:2016届四川省德阳市高三上学期10月月考理综化学试卷(解析版) 题型:填空题
Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + a Na2O2 = 2Na2FeO4 + b X + 2Na2SO4 + c O2↑
该反应中物质X应是 ________ ,b与c的关系是 _____________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式: ________________。
②每生成1mol FeO42-转移 _______mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 ______ mo1。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是________________________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为________________________(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.二氧化硅的结构式:O =Si= O
B.H2O沸点高于NH3,是因为H2O分子间存在氢键而NH3分子间不存在氢键
C.含有金属离子的晶体一定是离子晶体
D.分子晶体中一定存在分子间作用力,不一定存在共价键
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市高三上学期期中测试理综化学试卷(解析版) 题型:实验题
某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设①该反应的气体产物是CO2;②该反应的气体产物是CO。
③该反应的气体产物是 。
(2)设计方案,如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
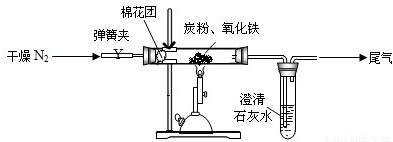
(3)查阅资料
氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气。
请写出该反应的离子方程式: 。
(4)实验步骤
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为 。
(5)数据处理
试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: 。
(6)实验优化 学习小组有同学认为应对实验装置进一步完善。
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 。
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期半期考试化学试卷(解析版) 题型:选择题
下列各组物质中,分类完全正确的一组是
A酸 | B碱 | C盐 | D氧化物 |
H2SO4 | Ba(OH)2 | H2S | H2O2 |
NaHCO3 | Cu2(OH)2CO3 | KCl | CO |
HNO3 | NaOH | CaCO3 | CuO |
HCl | Na2CO3 | CuSO4 | MnO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com