
| A. | ②⑤ | B. | ②④⑤ | C. | ④⑤⑧ | D. | 全部正确 |
分析 ①共价化合物是指只含有共价键的化合物;
②根据电解质是在水溶液中或熔融状态下能导电的化合物进行分析;
③高分子化合物是相对分子质量高达几万、几十万的物质;
④质子数相同,中子数不同的原子互称同位素;
⑤根据同素异形体是由同种元素形成的不同种单质进行分析;
⑥结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物;
⑦分子式相同结构不同的有机化合物互称同分异构体
⑧放热反应是产物的能量低于反应物的能量的反应,包括中和反应,大多化合反应,物质的燃烧反应等.
解答 解:①共价化合物:CO2、CCl4、CH3CH3,但是NH4NO3 属于离子化合物,故错误;
②明矾、冰醋酸、石膏、纯碱是在水溶液中或熔融状态下能导电的化合物,属于电解质,故正确;
③高分子化合物:淀粉,但是油脂、部分蛋白质不属于高分子化合物,故错误;
④1H2、2H2、3H2不是核素,不属于同位素,故错误;
⑤C60、C80、金刚石、石墨是碳元素的不同单质,属于同素异形体,故正确;
⑥CH2O2、C2H4O2、C3H6O2、C4H8O2不一定属于同一类物质,可能是羧酸和酯类,不是同系物的关系,故错误;
⑦乙二酸二乙酯、乙二酸乙二酯的分子式不同,不是同分异构体,故错误;
⑧盐酸与氢氧化钠、甲烷燃烧是放热反应,但是碳酸钙高温分解属于吸热反应,故错误.
故选A.
点评 本题考查物质的分类知识,熟记各类物质的概念是解决该题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| Ⅰ | Ⅱ | |
| A | 在淀粉KI试纸上滴几滴的FeCl3溶液,试纸变蓝 | 2Fe3++2I-=I2+2Fe2+ |
| B | 铝条置于火焰加热,看到铝熔化欲滴落,却又很快凝固 | 加热时,与O2发生反应,反应吸热 |
| C | 钠投到煤油和水的混合物中,钠粒在分界处作跳动和游动 | 钠的密度比水小比煤油大,能与水反应产生H2 |
| D | 一试管内有2V的Cl2,倒置于水中,在强光充分照射,最后试管中气体变为无色,体积为V | 因为反应Cl2+H2O?HCl+HClO 和2HClO$\stackrel{光照}{?}$2HCl+O2↑ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌是正极,铜是负极,电流的方向是从锌到铜 | |
| B. | 锌片质量减少,铜片质量增加 | |
| C. | 正极和负极上发生的都是氧化还原反应 | |
| D. | 原电池中的能量变化是:化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
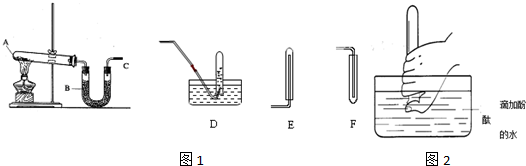
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.25NA | |
| B. | 常温常压下,6.4 g氧气和臭氧的混合气体中含有的原子总数为0.4NA | |
| C. | 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L | |
| D. | 常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
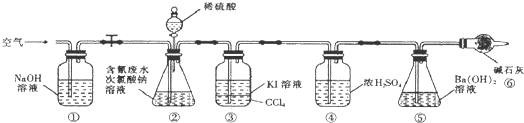
 “8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.
“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数( 25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
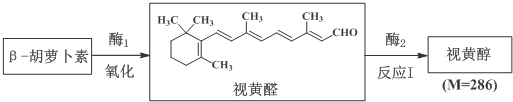
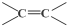 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$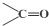 +
+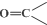
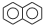 ,C10H8)的衍生物,其可能具有的化学性质有bd(选填编号).
,C10H8)的衍生物,其可能具有的化学性质有bd(选填编号).
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提高硫酸厂尾气的回收效率 | |
| B. | 强制燃煤企业完善脱硫设备 | |
| C. | 用天然气代替含硫的煤作民用燃料 | |
| D. | 减少全球工业化生产过程的CO2气体年排放总量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com