
分析 (1)依据配制溶液体积选择容量瓶规格,依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸的体积;
(2)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(3)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,据此排序;
(4)用量筒量取浓硫酸时,仰视量进行读数导致量取的浓硫酸体积偏大,定容时,仰视观察容量瓶刻度,导致溶液体积偏大,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)需配制450mL2mol/L的稀硫酸,应选择500mL容量瓶,实际配制500mL溶液,质量分数为98%密度为1.84g/mL的浓硫酸物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=2mol/L×500mL,解得V=54.3mL;
故答案为:54.3;
(2)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、移液、洗涤、定容、摇匀等,用到的仪器:量筒、烧杯、玻璃棒、容量瓶、胶头滴管,不需要的是:托盘天平、试管;
故选:AG;
(3)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的顺序为:DCAEBFHG;
故答案为:DCAEBFHG;
(4)用量筒量取浓硫酸时,仰视量进行读数导致量取的浓硫酸体积偏大,所含溶质硫酸的物质的量偏大,依据C=$\frac{n}{V}$可知溶液浓度偏高;
定容时,仰视观察容量瓶刻度,导致溶液体积偏大,依据C=$\frac{n}{V}$可知溶液浓度偏低;
故答案为:偏高;偏低.
点评 本题考查了一定物质的量浓度溶液的配制及有关物质的量浓度计算,明确配制原理及操作步骤是解题关键,注意熟练掌握物质的量与溶质质量分数的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 烧碱、纯碱、熟石灰都是碱 | B. | 铝土矿、水玻璃、小苏打都是混合物 | ||
| C. | Na2O、Al2O3、Fe2O3都是碱性氧化物 | D. | H2SO4、KOH、NaCl都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、NO3-、Br- | B. | Na+、NH4+、NO3-、Cl- | ||
| C. | K+、Na+、HCO3-、NO3- | D. | K+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | NaCl+AgNO3═NaNO3+AgCl↓ | D. | Zn+CuSO4═Cu+ZnSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
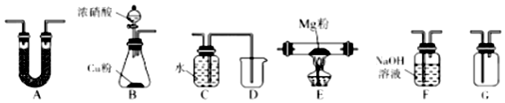
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
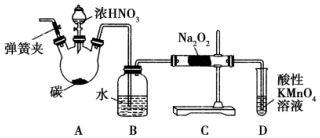 亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水为原料制备亚硝酸钠的装置如图所示.
亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水为原料制备亚硝酸钠的装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+NaHCO3→Na2CO3+H2O | |
| B. | Ca(OH)2+Ca(HCO3)2→2CaCO3↓+2H2O | |
| C. | 2NaOH+NH4HCO3→NH3?H2O+Na2CO3+H2O | |
| D. | NaOH+Ca(HCO3)2→2CaCO3↓+H2O+NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com