
 ,
, +AS
+AS| H+ |
 +CH3COOH
+CH3COOH
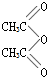
 酸化生成水杨酸,则水杨酸A的结构为
酸化生成水杨酸,则水杨酸A的结构为 ,水杨酸与乙酸酐发生信息中的取代反应生成阿司匹林B,则B为
,水杨酸与乙酸酐发生信息中的取代反应生成阿司匹林B,则B为 ,水杨酸发生缩聚反应生成高聚物G,则G为
,水杨酸发生缩聚反应生成高聚物G,则G为 .苯酚与足量的氢气发生加成反应生成D为
.苯酚与足量的氢气发生加成反应生成D为 ,D发生消去反应生成E为
,D发生消去反应生成E为 ,环己烯与溴发生加成反应生成
,环己烯与溴发生加成反应生成 ,由反应⑧产物结构可知,
,由反应⑧产物结构可知, 发生消去反应生成F为
发生消去反应生成F为 ,F发生加聚反应得到高聚物.水杨酸与D发生酯化反应生成C为
,F发生加聚反应得到高聚物.水杨酸与D发生酯化反应生成C为 ,据此解答.
,据此解答. 酸化生成水杨酸,则水杨酸A的结构为
酸化生成水杨酸,则水杨酸A的结构为 ,水杨酸与乙酸酐发生信息中的取代反应生成阿司匹林B,则B为
,水杨酸与乙酸酐发生信息中的取代反应生成阿司匹林B,则B为 ,水杨酸发生缩聚反应生成高聚物G,则G为
,水杨酸发生缩聚反应生成高聚物G,则G为 .苯酚与足量的氢气发生加成反应生成D为
.苯酚与足量的氢气发生加成反应生成D为 ,D发生消去反应生成E为
,D发生消去反应生成E为 ,环己烯与溴发生加成反应生成
,环己烯与溴发生加成反应生成 ,由反应⑧产物结构可知,
,由反应⑧产物结构可知, 发生消去反应生成F为
发生消去反应生成F为 ,F发生加聚反应得到高聚物.水杨酸与D发生酯化反应生成C为
,F发生加聚反应得到高聚物.水杨酸与D发生酯化反应生成C为 ,
, ,含有官能团的名称为:羟基、酯基,故答案为:羟基、酯基;
,含有官能团的名称为:羟基、酯基,故答案为:羟基、酯基; ,
, ;
; ,故答案为:
,故答案为: ;
; )的同分异构体符合:
)的同分异构体符合: 等,
等, 任意一种.
任意一种.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应过程中MnO2作催化剂 |
| B、盐酸未完全反应 |
| C、被还原的HCl少于0.2 mol |
| D、反应产生2.24 L氯气(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com