
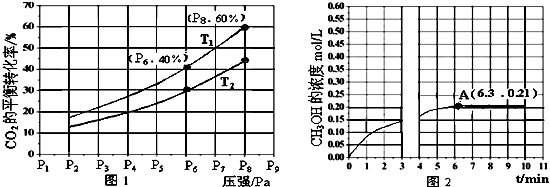
分析 (1)反应中产物气体数和小于反应物气体系数和,据此判断反应熵变符号;根据盖斯定律确定所求反应和已知反应之间的关系,计算反应的焓变即可;
(2)①反应达到平衡状态,各组分的浓度不随着时间的变化而变化,正逆反应速率相等,根据化学平衡状态的特征结合变量不变的状态是平衡状态来回答;
②反应是放热的,所以温度升高,平衡逆向进行,反应物的转化率降低,据此回答;
③根据三行式结合化学平衡常数表达式来进行计算即可;
a.据图示分析,改变外界条件新的平衡又会重新建立;
b.根据三行式结合化学平衡常数表达式来进行计算即可.
解答 解:(1)反应中产物气体数和小于反应物气体系数和,反应熵变小于零,反应①:CO2(g)+H2(g)=CO(g)+H2O(g)△H1=+41.19kJ•mol-1,反应②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H3=-49.58kJ•mol-1,反应CO(g)+2H2(g)=CH3OH(g)可以看成是②-①得到,所以反应焓变=-49.58kJ•mol-1-41.19kJ•mol-1=-90.77 kJ•mol-1,故答案为:<;-90.77 kJ•mol-1;
(2)①A.断裂3molH-H键,同时有2molH-O键形成,只能说明反应正向进行,不能说明正逆反应速率相等,此时的状态不一定平衡,故A正确;
B.CH3OH的浓度不再改变的状态是平衡状态的特征,故B错误;
C.容器中气体的平均摩尔质量等于质量和物质的量的比值,质量守恒,但是物质的量始终变化,所以当气体的平均摩尔质量不变的状态是平衡状态,故C错误;
D.容器中的反应是在恒压下进行的,当容器中气体的压强不变时,不一定是平衡状态,故D正确.
故选AD.
②反应Ⅲ为放热反应,温度降低,反应正向移动,二氧化碳的转化率升高,所以T1<T2,故答案为:<;应Ⅲ为放热反应,温度降低,反应正向移动,所以T1<T2;
③CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
初始量:1mol 3mol 0 0
变化量:0.4mol 1.2mol 0.4mol 0.4mol
平衡量:0.6mol 1.8mol 0.4mol 0.4mol
K=$\frac{\frac{0.4}{1.8}×\frac{0.4}{1.8}}{\frac{0.6}{1.8}×\frac{1.8}{1.8}}=0.148$
故答案为:0.148
a.结合图示的,改变的外界条件是降低压强,向气体体积增大的方向进行,故答案是降低压强;
b.CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
初始量:1mol 3mol 0 0
变化量:0.4mol 1.2mol 0.4mol 0.4mol
平衡量:0.6mol 1.8mol 0.4mol 0.4mol
K=$\frac{\frac{0.4}{1.8}×\frac{0.4}{1.8}}{\frac{0.6}{1.8}×(\frac{1.8}{1.8})^{3}}$=$\frac{4}{27}$=0.148
CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
初始量:1mol 3mol 0 0
变化量:0.6mol 1.8mol 0.6mol 0.6mol
平衡量:0.4mol 1.2mol 0.6mol 0.6mol
K=$\frac{\frac{0.6}{v}×\frac{0.6}{v}}{\frac{0.4}{v}×(\frac{1.2}{v})^{3}}$=$\frac{4}{27}$解得V=0.533
故答案为:0.553
点评 本题涉及化学平衡的判断、计算以及热化学方程式的书写知识,注意盖斯定律的应用是关键,难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 44g CO2含有的原子数目为 NA | |
| B. | 1L1 mol•L-1 的(NH4)2SO4 溶液中含有的 NH4+数目为2NA | |
| C. | 足量的 MnO2与 100mL12 mol•L-1的浓盐酸充分反应,转移的电子数目为 0.6 NA | |
| D. | 常温常压下,18mL 水含有的分子数目约为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化硼分子间含有氢键 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 氯化硼分子呈正三角形,属非极性分子 | |
| D. | 其分子空间结构类似CH4O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转化①有利于碳参与自然界的元素循环 | |
| B. | 转化②中S和O2属于不同的核素 | |
| C. | 可用澄清的石灰水鉴别CO2与SO2 | |
| D. | 转化的热化学方程式是:2CO(g)+SO2(g)═S(s)+2CO2 (g)△H=+270kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
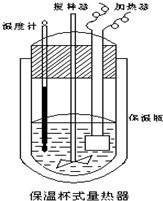 在如图所示的量热计中,将100mL0.50mol•L-1CH3COOH溶液与100mL0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,两溶液的密度均近似为1g•mL-1.下列说法错误的是( )
在如图所示的量热计中,将100mL0.50mol•L-1CH3COOH溶液与100mL0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,两溶液的密度均近似为1g•mL-1.下列说法错误的是( )| A. | CH3COOH溶液与NaOH溶液的反应为吸热反应 | |
| B. | 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和 | |
| C. | 若量热计的保温瓶绝热效果不好,则所测△H偏大 | |
| D. | CH3COOH的中和热△H为-53.3KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ;d的晶体类型是金属.
;d的晶体类型是金属.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com