
| A、方程式中产物CO2的计量数为6 |
| B、CO2是还原产物,ClO2是氧化产物 |
| C、氧化剂和还原剂的物质的量之比为4:1 |
| D、每生成1mol CO2需转移24mol电子 |


科目:高中化学 来源: 题型:
| A、碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、澄清石灰水与稀硝酸:Ca(OH)2+2H+═Ca2++2H2O |
| C、硫酸与氢氧化钡溶液:H+SO42-+Ba2++OH-═H2O+BaSO4↓ |
| D、小苏打与醋酸溶液反应:HCO3-+CH3COOH═CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | a | b | c | d | e | f | g |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -2 | +3 | +1 | +1 |
| A、氢氧化物碱性的强弱:g<f |
| B、由b与g两元素形成的化合物都属于离子化合物 |
| C、元素e的氧化物只能与酸反应 |
| D、沸点:a2b<a2d |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠 | B、水 |
| C、氢氧化钠溶液 | D、硝酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化镁与盐酸的反应:H++OH-═H2O |
| B、硝酸汞溶液和铝反应:3Hg2++2Al═2Al3++3Hg |
| C、MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ |
| D、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三种溶液pH的大小顺序是①>③>② |
| B、三种溶液中由水电离出的OH-浓度的大小顺序是①>②>③ |
| C、若将三种溶液稀释相同倍数,pH变化最大的是③ |
| D、若分别加入10mL 0.1mol?L-1盐酸后,pH最大的是② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 mol |
| B、8 mol |
| C、4 mol |
| D、3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

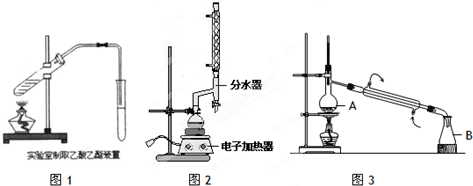
| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸* | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com