(2013?烟台模拟)CO与H
2二者发生如下的化学反应:CO(g)+2H
2(g)?CH
4O(g)△H<0,该反应的产物甲醇是化学工业重要的基础原料.
(1)该反应中氧化剂是
CO
CO
.相同温度下,1molCO完全燃烧的焓变为△H
1,1molCH
4O(g)完全燃烧的焓变为△H
2,则△H
1与△H
2的关系为△H
1>
>
△H
2(填“>”、“<”或“=”).
(2)一定温度下,将1molCO和2molH
2充入体积为2L的恒容密闭容器中,反应10min后达到平衡状态,测得CH
4O(g)的物质的量为0.6mol,则0~10min内的平均速率v(H
2)=
0.06mol/(L.min)
0.06mol/(L.min)
,化学平衡常数K=
9.375(mol/L)-2
9.375(mol/L)-2
.
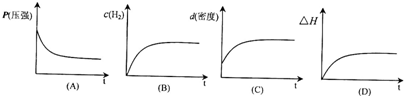
下列表示该反应过程的示意图正确的是
A
A
(填字母).
若开始在相同容积的密闭容器中充入2molCO和4molH
2,则反应达到平衡后,CO的转化率与原平衡相比
增大
增大
(填“增大”、“减小”、“不变”).
(3)①甲醇催化氧化得甲酸(HCOOH),甲酸是一种弱酸.25℃时配制pH为1的甲酸溶液,若加水稀释10倍,则
与稀释前比较
C
C
(填字母)
A.一定增大 B.一定减小 C.不变 D.可能增大 E.可能减小
②若将pH=1的HCOOH溶液和pH=1的HCl溶液等体积混合,则混合过程中,电离平衡HCOOH?HCOO
-+H
+的变化趋势是
C
C
(填字母).
A.向右移动 B.向左移动 C.不移动 D.无法判断
判断的依据是
混合后溶液中Qc=Ka
混合后溶液中Qc=Ka
.



