
【题目】目前,国家电投集团正在建设国内首座百千瓦级铁-铬液流电池储能示范电站。铁-铬液流电池总反应为Fe3++Cr2+![]() Fe2++Cr3+,工作示意图如图。下列说法错误的是
Fe2++Cr3+,工作示意图如图。下列说法错误的是

A.放电时a电极反应为Fe 3++e=Fe2+
B.充电时b电极反应为Cr3++e=Cr2+
C.放电过程中H+通过隔膜从正极区移向负极区
D.该电池无爆炸可能,安全性高,毒性和腐蚀性相对较低
【答案】C
【解析】
铁-铬液流电池总反应为Fe3++Cr2+![]() Fe2++Cr3+,放电时,Cr2+发生氧化反应生成Cr3+、b电极为负极,电极反应为Cr2+-e-=Cr3+,Fe3+发生得电子的还原反应生成Fe2+,a电极为正极,电极反应为Fe3++e-═Fe2+,放电时,阳离子移向正极、阴离子移向负极;充电和放电过程互为逆反应,即a电极为阳极、b电极为阴极,充电时,在阳极上Fe2+失去电子发、生氧化反应生成Fe3+,电极反应为:Fe2+-e-═Fe3+,阴极上Cr3+发生得电子的还原反应生成Cr2+,电极反应为Cr3++e-═Cr2+,据此分析解答。
Fe2++Cr3+,放电时,Cr2+发生氧化反应生成Cr3+、b电极为负极,电极反应为Cr2+-e-=Cr3+,Fe3+发生得电子的还原反应生成Fe2+,a电极为正极,电极反应为Fe3++e-═Fe2+,放电时,阳离子移向正极、阴离子移向负极;充电和放电过程互为逆反应,即a电极为阳极、b电极为阴极,充电时,在阳极上Fe2+失去电子发、生氧化反应生成Fe3+,电极反应为:Fe2+-e-═Fe3+,阴极上Cr3+发生得电子的还原反应生成Cr2+,电极反应为Cr3++e-═Cr2+,据此分析解答。
A.根据分析,电池放电时a为正极,得电子发生还原反应,反应为Fe3++e=Fe2+,A项不选;
B.根据分析,电池充电时b为阴极,得电子发生还原反应,反应为Cr3++e=Cr2+,B项不选;
C.原电池在工作时,阳离子向正极移动,故放电过程中H+通过隔膜从负极区移向正极区,C项可选;
D.该电池在成充放电过程中只有四种金属离子之间的转化,不会产生易燃性物质,不会有爆炸危险,同时物质储备于储液器中,Cr3+、Cr2+毒性比较低,D项不选;
故答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下图是我国学者研发的高效过氧化氢一尿素电池的原理装置:
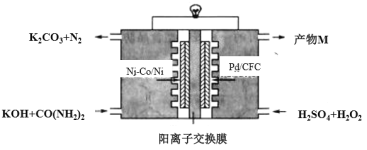
该装置工作时,下列说法错误的是
A.Ni-Co/Ni极上的电势比Pd/CFC极上的低
B.向正极迁移的主要是K+,产物M主要为K2SO4
C.负极反应为:CO(NH2)2+8OH–-6e–=CO32–+N2↑+6H2O
D.Pd/CFC极上发生反应:H2O2+2e–=2OH–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如右所示。下列关于分枝酸的叙述正确的是( )

A. 可与乙醇、乙酸反应,且反应类型相同
B. 分子中含有2种官能团
C. 1mol分枝酸最多可与3mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别放在0.1 molL-1H2SO4溶液中的四块相同的纯锌片,其连接情况如图所示:

(1)其腐蚀速率由快到慢的顺序是________;
(2)写出②号内正极发生的电极反应式_________;
(3)若③号烧杯内的电解质溶液为NaCl溶液,则Zn电极发生的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有相同电子层数、原子序数相连的三种元素X、Y、Z,最高价氧化物对应水化物的酸性相对强弱是:![]() ,则下列判断正确的是()
,则下列判断正确的是()
A.形成的气态氢化物的稳定性:X<Y<Z
B.原子半径:X>Y>Z
C.原子序数:X>Y>Z
D.得电子能力:X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中正确的是( )
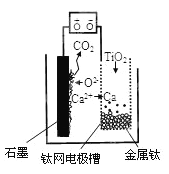
A. 将熔融CaF2—CaO换成Ca(NO3)2溶液也可以达到相同目的
B. 阳极的电极反应式为:C+2O2--4e-=CO2↑
C. 在制备金属钛前后,整套装置中CaO的总量减少
D. 石墨为阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:
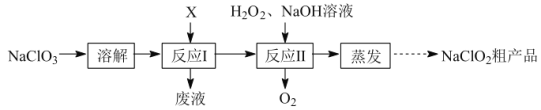
已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
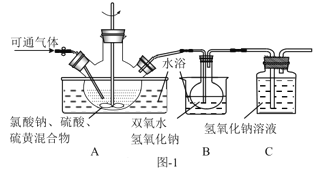
①若X为硫磺与浓硫酸,也可反应生成ClO2。该反应较剧烈。若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
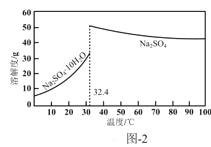
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图2所示。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下使NH2COONH4 ( s) ![]() 2NH3 (g)+CO2 (g)达到平衡,不可以判断该反应达到化学平衡的是 ( )
2NH3 (g)+CO2 (g)达到平衡,不可以判断该反应达到化学平衡的是 ( )
A. V正(NH3) =2V逆(CO2)B. 密闭容器中氨气的体积分数不变
C. 密闭容器中总压强不变D. 密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知合成二甘醇的原理为:![]() +HOCH2CH2OH
+HOCH2CH2OH![]() HOCH2CH2OCH2CH2OH,下列叙述正确的是( )
HOCH2CH2OCH2CH2OH,下列叙述正确的是( )
A. 二甘醇能与氢气发生加成反应
B. 二甘醇是乙醇的同系物
C. 二甘醇是丙二醇(C3H8O2)的同分异构体
D. 二甘醇能通过脱水产生碳碳双键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com