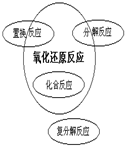
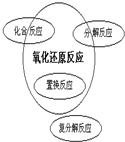
�������ƣ�NaNO
2����һ�������ʳ�����Ƶ�ʳƷ���Ӽ���ij��ѧ��ȤС���������ʵ�飮
��ʵ��I��
������װ�ã���ʡ�Լг�װ�ã���NaNO
2��
��֪��2NO+Na
2O
2�T2NaNO
2��2NO
2+Na
2O
2�T2NaNO
3��
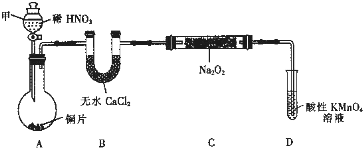
��1��������������
��װ��B��������
��
��2��װ��D�ɽ�ʣ���NO������NO
3-��������Ӧ�����ӷ���ʽΪ
��
��3��ʹ�����������õ�����װ�ý���ʵ�飬NaNO
2�Ĵ��Ƚϵͣ�Ϊ���NaNO
2�����������ʵ��װ�û�ҩƷ���иĽ�����Ľ���ʩ��
��
��ʵ���
����Ŀ�ӱ�ɫ�����Ƚ���Һ��ɫ��dz�Բⶨ����Ũ�ȣ��ⶨ�ݲ���Ʒ��NaNO
2�����
����i����5���б�ŵ��Թ��зֱ���벻ͬ����NaNO
2��Һ��������1mL��M��Һ��M��NaNO
2���Ϻ�ɫ��NaNO
2Ũ��Խ����ɫԽ����ټ�����ˮ���������Ϊl0mL�����Ƴɱ�ɫ�ף�
| �Թܱ�� | �� | �� | �� | �� | �� |
| NaNO2����/mg?L-1 | 0 | 20 | 40 | 60 | 80 |
����ii��1kg�ݲ���Ʒ
��Һ
��Һ
����ҺX
���袣��ȡ5mL����ҺX������1mL M��Һ��������ˮ��10mL�����ɫ�ױȽϣ�
��4������ii��ȡ����ҺX�Ĺ����У�����������Ŀ����
��
��5������iii�ȽϽ����ܺ�ɫ����ɫ��ͬ�����ݲ���Ʒ��NaNO
2�ĺ���Ϊ
mg?kg
-1��6����Ŀ�ӱ�ɫ��֤���ݲ��м���ά����C���Խ���NaNO
2�ĺ�������Ʋ��������ʵ�鱨�森
| ʵ�鷽�� | ʵ������ | ʵ����� |
| | ά����C���Խ����ݲ���NaNO2�ĺ��� |