
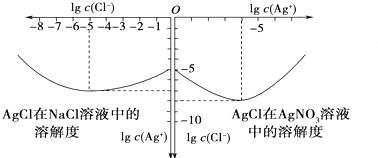
| c(Br-) |
| c(Cl-) |
| c(Br-) |
| c(Cl-) |
| Ksp(AgBr) |
| Ksp(AgCl) |
| Ksp(AgBr) |
| c(Ag+) |
| Ksp(AgCl) |
| c(Ag+) |
| c(Br-) |
| c(Cl-) |
| Ksp(AgBr) |
| Ksp(AgCl) |
| 5.4×10-13 |
| 2.0×10-10 |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
| A、1 mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、在25℃、101 kPa时,22.4 L氢气中含有NA个氢分子 |
| C、常温常压下,11.2LN2中含有的分子数为0.5NA |
| D、1L 0.5mol?L-1Na2SO4溶液中含有的钠离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无机非金属材料可能含有金属元素;人工合成尿素彻底推翻了“生命力论”,使得有机化学得到迅猛发展 |
| B、元素分析仪不仅可以检验C、H、O、N、S等非金属元素,还可以检验Cr、Mn等金属元素 |
| C、改变金属组成和结构的电化学方法可以较好的防治硫酸型酸雨对金属的腐蚀 |
| D、在化学反应过程中,原子核一定不发生变化,但最外层电子数不一定改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下将pH=3的酸HR溶液与pH=11的NaOH溶液等体积混合,若测得pH≠7,则混合溶液的pH>7 |
| B、在0.1mol/L的Na2S溶液中存在:c(OH-)=c(HS-)+c(H2S)+c(H+) |
| C、向Na2CO3粉末中滴加硼酸溶液,有CO2产生 |
| D、自然界各种原生铜的硫化物经氧化、淋滤作用后变为CuSO4溶液,遇到深层的闪锌矿(ZnS)和方铅矿(PbS)可转变为铜蓝(CuS),说明CuS的溶度积小于ZnS、PbS |
查看答案和解析>>
科目:高中化学 来源: 题型:
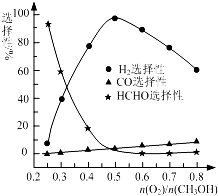 甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.| 1 |
| 2 |
| 1 |
| 2 |
| n(O2) |
| n(CH3OH) |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ksp只与难溶电解质本身的性质和温度有关 |
| B、在一定温度下的AgCl饱和溶液中,C(Ag+)和C(Cl-)的乘积是一个常数 |
| C、在一定温度下,向AgCl饱和溶液中加入盐酸时,Ksp值变大 |
| D、由于Ksp(FeS)>Ksp(CuS),所以FeS沉淀在一定条件下可以转化为CuS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com