
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0.20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为 , 表中bc(填“<”、“=”、“>”).
(2)20s时,N2O4的浓度为mol/L,0~20s内N2O4的平均反应速率为 .
(3)该反应的平衡常数表达式K= , 在80℃时该反应的平衡常数K值为(保留2位小数).
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 . A、N2O4的转化率越高 B、NO2的产量越大
C、N2O4与NO2的浓度之比越大 D、正反应进行的程度越大.
【答案】
(1)N2O4?2NO2;>
(2)0.14;0.003mol/L?s
(3)![]() ;0.54
;0.54
(4)A、B、D
【解析】解:(1)将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,反应的化学方程式为:N2O42NO2 , 隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;依据化学平衡三段式列式计算分析判断;进行到40S和进行到60S时;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
变化量(mol) | 0.2 | 0.4 | |
40S末(mol) | 0.2 | 0.4 |
得到b=0.2mol/L;
进行到60S和进行到60S时;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
变化量(mol) | 0.22 | 0.44 | |
60S末(mol) | 0.18 | 0.44 |
c=0.18 mol/L
计算比较得到,b>c;
故答案为:N2O42NO2;>;(2)进行到20S;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
变化量(mol) | 0.12 | 0.24 | |
60S末(mol) | 0.28 | 0.24 |
20s时,N2O4的浓度= ![]() =0.14mol/L;
=0.14mol/L;
0~20s内N2O4的平均反应速率= ![]() =0.003mol/Ls;
=0.003mol/Ls;
故答案为:0.14;0.003mol/Ls;(3)N2O42NO2 , 平衡常数K= ![]() ;
;
80°C平衡状态和60S是相同平衡状态,平衡浓度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L;
平衡常数K= ![]() =
= ![]() =0.54mol/L;
=0.54mol/L;
故答案为: ![]() ;0.54;(4)反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;该反应的K值越大,说明平衡正向进行,是温度降低的原因;
;0.54;(4)反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅,说明反应逆向进行,逆向是放热反应,正向是吸热反应;该反应的K值越大,说明平衡正向进行,是温度降低的原因;
A、平衡正向进行N2O4的转化率越高,故A正确;
B、平衡正向进行NO2的产量越大,故B正确;
C、依据上述计算分析平衡正向进行,N2O4与NO2的浓度之比越小,故C错误;
D、该反应的K值越大,说明平衡正向进行,正反应进行的程度越大,故D正确;
故答案为:ABD.
(1)依据反应条件分析判断,结合化学平衡的三段式列式计算分析比较;(2)化学平衡的三段式列式计算,结合化学反应速率概念计算0~20s内N2O4的平均反应速率;(3)依据化学方程式和平衡常数概念写出平衡常数表达式,依据80°C平衡状态下结合三段式列式计算平衡浓度计算平衡常数.


 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】A~J是常见的化学物质,转化关系如下图所示。A是生活中的一种调味剂,I是一种用途广泛的金属,常温下C、D、E、F、J皆为气体, H由两种元素构成,摩尔质量为41 g·mol-1。

(1)I的化学式为________,H的化学式为________。
(2)写出反应①②③④的化学方程式
①_______;②________; ③_______; ④________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.01mol/L的HA溶液中逐滴加入0.02mol/L的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( ) 
A.在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OHˉ)+c(Aˉ)
B.HA为弱酸
C.常温下,MA溶液的pH>7
D.N点水的电离程度小于K点水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是( )
A.Ag+、SO42﹣、Cl﹣
B.Fe2+、H+、NO3﹣
C.K+、Na+、NO3﹣
D.Mg2+、SO42﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需用2 mol·L-1氯化钠溶液450 mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是
A. 450 mL,52.7g B.500 mL,58.5g
C.1000 mL,117g D.任意规格,111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g)△H<0,若起始时c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒容的密闭容器中充入 0.1mol/L CO2、0.1mol/L CH4 , 在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( ) 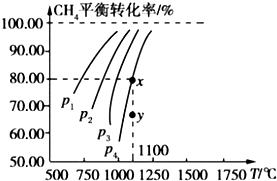
A.1100℃时该反应平衡常数为 1.64
B.压强:p4>p3>p2>p1
C.上述反应的△H<0
D.压强为 p4时,在y点:v 正>v 逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.常温下,铝片与浓硝酸不反应
B.Fe(OH)2是灰绿色的难溶固体
C.用激光笔照射胶体可产生“丁达尔效应”
D.标准状况下,22.4L CCl4中含有的分子数为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com