
已知电极上每通过96 500 C的电量就会有1 mol电子发生转移。精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中,常用银电量计,如图所示。下列说法不正确的是

A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag++e-= Ag
B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96.5 C
C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会偏高。
D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连。
【考点】本题考查电解原理的应用,注意电解池的组成和两极上的变化,并注意与电镀知识的结合来分析解答即可。
【解析】A、电解时的电极反应为:阳极(Ag):Ag-e-═Ag+,阴极(Pt):Ag++e-═Ag,故A正确;
B、析出Ag的物质的量为 =1mmol=0.001mol,根据Ag++e-=Ag可知通过电量为96.5库伦,故B正确;
=1mmol=0.001mol,根据Ag++e-=Ag可知通过电量为96.5库伦,故B正确;
C、银溶解时有些可能未失电子变成银离子然后在阴极(铂坩埚)得电子析出,而是直接跌落到铂坩埚中,造成铂坩埚增重较多,导致计算出的电量偏大,所以必须增加收集袋,故C正确;
D、要将银电量计与电解食盐水的电解池串联,才能做到通过的电量相同.所以电源正极接电解食盐水的电解池(待测电解池)的阳极,再从电解食盐水的电解池(待测电解池)的阴极连接到银电量计的银棒,然后再从铂坩埚接到电源的负极,故D错误。故选D。
【答案】D


科目:高中化学 来源: 题型:
现有以下5种说法:①胶体是纯净物;②盐酸和食醋既是化合物又是酸;③次氯酸、烧碱、纯碱依次分别为酸、碱、盐;④青铜器、钱币等均是合金;⑤CO为酸性氧化物。其中错误的是
A.①②⑤ B.①②③④⑤
C.③④ D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是( )

A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的酸性均减弱
D.产生气泡的速率甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室利用如右图装置进行中和热的测定。
 回答下列问题:
回答下列问题:
①如图装置中,为了酸碱能更充分地反应,应该增加一个 (填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会
(填“偏大”、“偏小”或“无影响”)。
②在操作正确的前提下提高中和热测定的准确性的关键是 ( 填代号)
A.进行实验时的气温
B.装置的保温隔热效果
C.实验所用酸碱溶液的体积
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将 (填“偏大”、“偏小”、“不变”);原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4 ( g ) + H2O ( g )=CO ( g ) + 3H2 ( g )
II:CO ( g ) + 2H2 ( g )=CH3OH ( g )
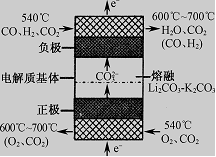
(1)反应(I)制得的混合气体和水煤气成分相同,也能形成燃料电池。下图是利用其作原料,采用熔融碳酸盐为电解质的燃料电池工作原理示意图,则该电池的负极反应式可表示为:
。
(2)在使用甲醇时,若有残留,对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:

①写出阳极电极反应式 。
②写出除去甲醇的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关浓硫酸与浓硝酸的叙述,不正确的是
A.露置空气中,两者浓度均降低 B常温下,两者均能使铁、铝钝化
C.一定条件下,两者均能与铜反应 D两者都具有强氧化性,均能氧化SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
将某份铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝物质的量之比为
A.3∶2 B.2∶1
C.3∶4 D.4∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com