
【题目】有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42﹣ HCO3﹣ NO3﹣ OH﹣ |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B ,D 。
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(3)在A溶液中加少入量澄清石灰水,其离子方程式为 。
(4)C常用作净水剂,用离子方程式表示其净水原理 。
【答案】(1)KNO3;CuSO4(2)Na2CO3
(3)Ca2++2HCO3-+2OH-==CaCO3↓+CO32-+2H2O
(4)Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
【解析】
试题分析:根据题意知D为蓝色溶液,说明D中含有铜离子;将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解,说明E是强碱,C中含有铝离子;进行焰色反应,仅有B、C为紫色,说明B、C中含有钾离子;根据实验④可知,A中含有HCO3-,C、D中含有SO42-,所以A是碳酸氢钠,C是硫酸铝钾,D是硫酸铜,E是氢氧化钠;将B、D两溶液混合,未见沉淀或气体生成,所以B是硝酸钾。
(1)B、D的化学式:B: KNO3,D:Na2CO3。
(2)碳酸氢钠和氢氧化钠反应的方程式是HCO3- + OH- = CO32- +H2O,该化合物的化学式是Na2CO3。
(3)石灰水不足时,生成物时碳酸钙、碳酸钠和水,离子方程式是Ca2++2HCO3-+2OH-==CaCO3↓+CO32-+2H2O。
(4)硫酸铝钾溶于水电离出的铝离子,水解生成氢氧化铝胶体,钠吸附水中的悬浮物,从而净水,方程式是Al3++3H2O![]() Al(OH)3+3H+。
Al(OH)3+3H+。


科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO![]() 及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.⑤④①②③ B.④①②⑤③ C.⑤②④①③ D.①④②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
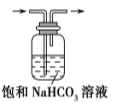
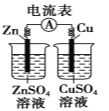
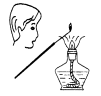
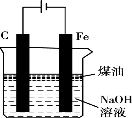
图(1) 图(2) 图(3) 图(4)
A.图(1)用于除去CO2中的HCl气体
B.图(2)表示已组装的铜锌原电池
C.图(3)观察钾的焰色反应
D.用图(4)装置制备Fe(OH)2并能较长时间观察其颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出除去下列物质中杂质所选用的试剂及发生反应的离子方程式:
(1)盐酸(硫酸),试剂_________,离子方程式__________________________;
(2)NaOH(Na2CO3),试剂________,离子方程式___________ _________ ___;
(3)NaCl(CuCl2),试剂________,离子方程式_______________________ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生。某兴趣小组对摩擦剂成分及其含量进行以下探究:
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是______________。
(2)往(1)所得滤液中通入过量二氧化碳,主要发生反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
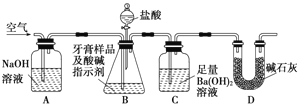
依据实验过程回答下列问题:
(3)D装置的作用是 ;
(4)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:______________。
(5)下列各项措施中,不能提高测定准确度的是________________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已经部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,经如下处理:

下列说法不正确的是
①滤液A中的阳离子为Fe2+、Fe3+、H+
②V=224mL ③V=336mL
④样品中含氧元素的物质的量为0.03mol
⑤溶解样品的过程中消耗硫酸的总物质的量为0.04mol
A. ①③ B. ①③④ C. ②④⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.一定条件下,0.2 mol SO2与足量O2充分反应,生成SO3分子数为0.2NA
B.0. 1 mol NH2— 中含有的电子数为0.9NA
C.3.4 g H2O2中含有的共用电子对数为0.1NA
D.常温常压下,16 g O2和O3混合气体含有的氧原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
①铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线拧在一起
②汽车尾气中含有能污染空气的氮氧化物,主要是汽油燃烧不充分造成的
③从海水中提取物质都必须通过化学反应才能实现
④“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料
⑤明矾可以用于净水,主要是由于Al3+水解生成的少量氢氧化铝胶体有净水作用
A.②③⑤ B.①②④ C.①③④⑤ D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com