
| A. | 质量相等的O2和O3中所含原子数相等 | |
| B. | 物质的量相等的O2和O3中所含分子数相等 | |
| C. | 物质的量相等的CO和CO2中所含原子数相等 | |
| D. | 物质的量相等的CO和CO2中所含碳原子数相等 |
分析 A.二者都只含有氧元素,根据n=$\frac{m}{M}$可知二者含有氧原子数相等;
B.根据N=nNA可知二者物质的量相等时含有分子数相同;
C.二者分子中含有原子数不同,则物质的量相等时含有原子数不同;
D.二者分子中含有含有1个碳原子,则物质的量相等时含有的碳原子数相等.
解答 解:A.质量相等的O2和O3中含有相同质量的O原子,则含有原子数相等,故A正确;
B.根据N=nNA可知,物质的量相等的O2和O3中所含分子数相等,故B正确;
C.CO和CO2分子中分别含有2、3个原子,根据N=nNA可知物质的量相等的CO和CO2中所含原子数不相等,故C错误;
D.物质的量相等的CO和CO2中所含碳原子的物质的量相等,根据N=nNA可知二者含有C原子数相等,故D正确;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
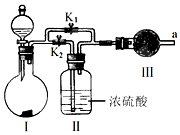
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C12按体积比1:3混合可制得纯净的CHCl3 | |
| B. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| C. | C3H6O2有3种同分异构体,它们均能与钠反应放出氢气 | |
| D. | 人体内的蛋白质分解,最终生成二氧化碳和水排出体外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
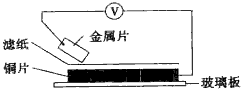 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如表 | 金属 | 电子流动方向 | 电压 |
| 甲 | 甲→Cu | +0.78 |
| 乙 | Cu→乙 | +0.15 |
| 丙 | 丙→Cu | +1.35 |
| 丁 | 丁→Cu | +0.30 |
| A. | 在四种金属中乙的还原性最强 | |
| B. | 金属乙能从硫酸铜溶液中置换出铜 | |
| C. | 甲、丁若形成原电池时,甲为负极 | |
| D. | 甲、乙形成合金在空气中,乙先被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②⑥⑧ | C. | ②③⑤⑦⑧ | D. | ①②④⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
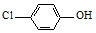 )的废水可以利用微生物电池除去,其原理如图1所示.
)的废水可以利用微生物电池除去,其原理如图1所示.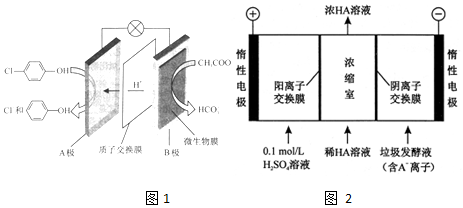
 -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-
-OH+Cl-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、NO、CO、烟尘 | B. | CO2、Cl2、N2、雾 | C. | HCl、NO2、N2、粉尘 | D. | CO2、NO、NH3、H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com