
| A. | 放电时负极反应式为:Zn-2e-=Zn2+ | |
| B. | 放电时每转移3mol电子,正极有2 mol K2FeO4被还原 | |
| C. | 放电时正极反应式为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- | |
| D. | 放电时正极附近溶液的碱性减弱 |
分析 高铁电池放电时,锌在负极失去电子,电极反应式为Zn-2e-+2OH-=Zn(OH)2,高铁酸钠在正极得到电子,电极反应式为2FeO42-+6e-+8H2O═2Fe(OH)3+10OH-,据此分析解答.
解答 解:A.放电时,锌失电子发生氧化反应,电极反应式为Zn-2e-+2OH-=Zn(OH)2,故A错误;
B.该电池反应式中,Fe元素化合价由+6价变为+3价,所以每转移3 mol 电子,正极有1 mol K2FeO4被还原,故B错误;
C.放电时正极得电子发生还原反应,所以正极反应式为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH-,故C正确;
D.根据正极反应式为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH-,所以正极附近溶液的碱性增强,故D错误;
故选C.
点评 本题考查化学电源新型电池,为高频考点,会根据元素化合价变化确定各个电极上发生的反应,难点是电极反应式的书写,易错选项是B.


科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子:${\;}_{6}^{12}$C | B. | HClO的结构式:H-Cl-O | ||
| C. | N2H4的电子式: | D. | 甲酸的分子式:CH2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
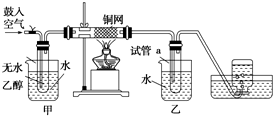 某实验如图.
某实验如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg | B. | Fe | C. | Al | D. | Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体密度恒定不变 | B. | 混合气体的颜色不再改变 | ||
| C. | 混合气体的平均摩尔质量恒定不变 | D. | H2、I2、HI的浓度相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com