
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
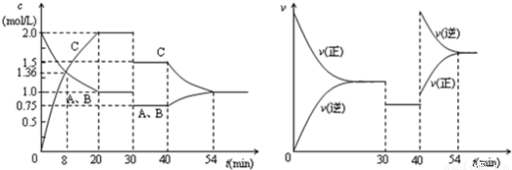
A.30min时降低温度,40min时升高温度
B.反应方程式中的x=1,正反应为吸热反应
C.8min前A的平均反应速率为0.08mol/(Lmin)
D.30min~40min间该反应使用了催化剂
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年江苏省南通、扬州、连云港高三第二次调研测试化学试卷(解析版) 题型:选择题
25℃时,向10 mL 0.1 mol·L-1 CH3COONa溶液中加入0.1 mol·L-1盐酸,溶液pH随加入盐酸的体积变化情况如图所示。下列说法正确的是
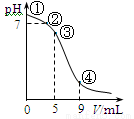
A.点①所示溶液中:c(OH-)=c(H+)+c(CH3COOH)
B.点②所示溶液中:c(CH3COOH)+c(CH3COO-)=0.05 mol·L-1
C.点③所示溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.点④所示溶液中:c(Na+)+c(H+)<c(CH3COO-)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
[化学──选修3 :物质结构与性质](15分)X、Y 、Z、W为元素周期表前四周期的元素。其中X原子核外的L层电子数是K层电子数的两倍, Y的内层电子数是最外层电子数的9倍,Z在元素周期表的各元素中电负性最大,W元素的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题。
(1)W元素属于 区元素,其基态原子的电子排布式为 。
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。其中配体分子的空间构型为 ,写出该配离子的结构简式(标明配位键) 。
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为 ,1 mol 该分子中σ键的数目为 ,该物质易溶于水的主要原因是 。
(4)X的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为 。
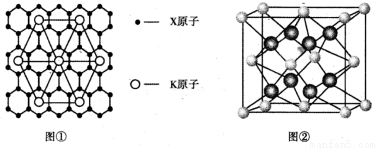
(5)元素Y与元素Z形成的晶体结构如图②所示,设晶胞中最近的Y的离子与Z的距离为a pm,该化合物的摩尔质量为bg/ mol ,则该晶胞密度的计算式为 g/cm3。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:简答题
(14分)BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等。工业上可用H2与重晶石(BaSO4)在高温下反应制备BaS,热化学方程式为BaSO4(s)+4H2(g) BaS(s)+4H2O(g)
BaS(s)+4H2O(g)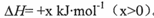 。回答下列问题:
。回答下列问题:
(1)在温度和容积不变的条件下,能说明该反应己达到平衡状态的是 (填字母序号)。
a.n(H2)=n(H2O)
b.容器内压强保持不变
c.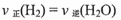
d.水蒸气的浓度保持不变
(2)平衡后下列措施既可提高反应速率,又可提高H2的转化率的是 (填字母序号)。
a.使用催化剂
b.升高反应体系的温度
c.增大反应容器的体积
d.及时从反应体系中分离出水蒸气
(3)将温度恒定为T℃,向体积为2L的密闭容器中加入一定量的重晶石和H2。在不同时间测得H2的物质的量如下表:

①2t时,n 1.20(填“>”、“<”或“=”)
②若氢气的平衡转化率为a,则该温度下反应的化学平衡常数K= (用含a的
代数式表示);若测得该反应达到平衡时吸热Q kJ ,则x= (用含a、Q的代数式表示)。
(4)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一固定容积的密闭容器中加入一定量的重晶石和H2,设计了下表中的三组实验:
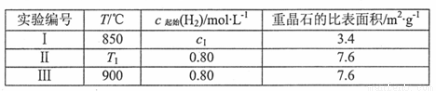
①填写上表中的实验条件: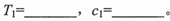
②在直角坐标系中画出I, II两组实验氢气的浓度随时间变化趋势图,并在每条曲线上标明对应的实验编号。
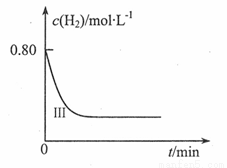
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.铝制容器可长期盛放酸性或碱性物质
B.甲烷会导致某些温泉有臭鸡蛋气味
C.太阳能的开发利用可降低碳排放量
D.塑料垃圾会造成水体富营养化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查(二)化学试卷(解析版) 题型:简答题
(14分)氮及其化合物在工农业生产、生活中有重要作用。请按要求回答下列相关问题:
(1)食品添加剂铵明矾NH4Al(SO4)2·12H2O高温可分解,下列关于其分解产物的预测不合理的是_____。
A.NH3、N2、SO2、H2O B.NH3、SO3、H2O
C.NH3、SO2、H2O D.NH3、N2、SO3、SO2、H2O
(2)汽车发动机工作时也会引发N2和O2反应产生大气污染物NO,其能量变化示意图为_____
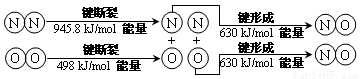
则该反应的热化学方程式为_________________________。
(3)工业合成氨的反应:N2(g)+3H2(g) 2NH3(g) △H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
2NH3(g) △H<0,分别在T1、T2温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
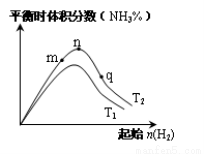
①比较在m、n、q三点所处的平衡状态中,反应物N2的转化率最高的是________点。
②T2条件下,在2 L的密闭容器中,充入x mol N2和y mol H2时,3 min达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):v(N2)=_______;该反应的平衡常数的值K =_______。
③图像中T2________T1(填“高于”、“低于”、“等于”或“无法确定”)。
④科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,这提高了氮气和氢气的转化率。写出电化学合成过程中发生还原反应的电极方程式:___________________________________。
(4)将质量相等的四份铁粉和铜粉的均匀混合物,分别加入同浓度稀硝酸充分反应,(假设硝酸的还原产物只有NO)实验数据如下表:
编 号 | ① | ② | ③ | ④ |
稀硝酸体积/mL | 100 mL | 200 mL | 300 mL | 400 mL |
剩余金属/g | 18.0 g | 9.6 g | 0 | 0 |
NO体积/L(标准状况下) | 2.24 L | 4.48 L | 6.72 L | V |
下列有关分析推断正确的是____________。
A.硝酸起始浓度为4 mol/L B.①中溶解了5.6 g Fe
C.③中n(Cu2+) = 0.15 mol D.④中V = 6.72 L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查(二)化学试卷(解析版) 题型:选择题
下列关于下图所示电化学装置的分析正确的是
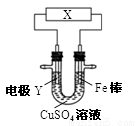
A.若X为直流电源,Y为铜棒接正极,则Fe棒上镀铜
B.若X为直流电源,Y为碳棒接负极,则Fe棒被保护
C.若X为电流计,Y为锌棒,则SO42- 移向Fe棒
D.若X为导线,Y为铜棒,则Fe棒发生还原反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期第二次月考化学试卷(解析版) 题型:选择题
一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是
A.该反应的正反应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
在高温高压的水溶液中,AuS-与Fe2+发生反应沉积出磁铁矿(主要成分Fe3O4)和金矿(含Au),并伴有H2S气体生成。对于该反应的说法一定正确的是
A.氧化剂和还原剂的物质的量之比2:3
B.AuS-既作氧化剂又作还原剂
C.每生成2.24 L气体,转移电子数为0.1mol
D.反应后溶液的pH值降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com