
在一个体积为2L的容器中,充入4mol CO和4mol H2O,一段时间后反应CO(g)+H2O(g)⇌CO2(g)+H2(g)在密闭容器中达到了平衡状态.平衡后c[CO2]=1.8mol•L﹣1,则该温度下此反应的平衡常数K为( )
|
| A. | 27 | B. | 36 | C. | 54 | D. | 81 |
考点:
化学平衡的计算.
专题:
化学平衡专题.
分析:
化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,可逆反应CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数k= ,根据三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算.
,根据三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算.
解答:
解:平衡后c(CO2)=1.8mol•L﹣1,则:
CO(g)+H2O(g)⇌CO2(g)+H2(g)
开始(mol/L):2 2 0 0
变化(mol/L):1.8 1.8 1.8 1.8
平衡(mol/L):0.2 0.2 1.8 1.8
故该温度下平衡常数k= =
= =81,
=81,
故选D.
点评:
本题考查化学平衡常数的有关计算,难度不大,注意三段式解题法的利用,书写化学平衡常数是关键.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇: CO(g)+2H2(g) 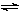 CH3OH(g)。如图是该反应在不同温度下CO的转化率随时间变化的曲线。下列判断正确的是
CH3OH(g)。如图是该反应在不同温度下CO的转化率随时间变化的曲线。下列判断正确的是
A.T1>T2
B.该反应的△H >0
C.T1时的平衡常数K1> T2时的平衡常数K2
D.T1时的平衡常数K1< T2时的平衡常数K2
查看答案和解析>>
科目:高中化学 来源: 题型:
有关常温下pH均为3的醋酸和硫酸的说法正确的是 ( )
A.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol/L
B.分别加水稀释100倍后,两种溶液的pH仍相同
C.醋酸中的c(CH3COO-)和硫酸中的c(SO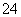 )相等
)相等
D.分别加入足量锌片,两种溶液生成H2的体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体⑤加NaCl溶液 ⑥滴加几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)⑧改用10mL 0.1mol/L的盐酸.
|
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ③⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | pH=2与pH=1的硝酸中c(H+)之比为1:10 |
|
| B. | Na2CO3溶液中c(Na+)与c(CO32﹣)之比为2:1 |
|
| C. | 0.2 mol•L﹣1与0.1mol•L﹣1醋酸中c (H+)之比为2:1 |
|
| D. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在给定的四种溶液中加入以下各种离子,各离子能在原溶液中共存的是( )
|
| A. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl﹣、SCN﹣ |
|
| B. | pH为1的溶液:Cu2+、Na+、Mg2+、NO3﹣ |
|
| C. | 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+ |
|
| D. | 所含溶质为Na2SO4的溶液:K+、CO32﹣、NO3﹣、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学平衡原理在工农业生产中发挥着重要的指导作用.
(1)反应C(s)+CO2(g)⇌2CO(g)平衡常数K的表达式为 = ;已知C(s)+H2O(g)⇌CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)⇌CO(g)+H2O(g)的平衡常数为K2,则K与K1、K2二者的关系为 .
(2)已知某温度下,反应2SO2(g)+O2 (g)⇌2SO3(g),的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1mol•L﹣1,C(O2)=1mol•L﹣1,当反应在该温度下SO2转化率为80%时,该反应 (填“是”或“否”)达到化学平衡状态,若未达到,向 (填“正反应”或“逆反应”) 方向进行.
(3)对于可逆反应:aA(g)+bB(g)⇌cC(g)+dD(g)△H=a kJ•mol﹣1;若a+b>c+d,增大压强平衡向 (填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a 0(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3+Cl2⇌PCl5.达平衡时,PCl5为0.40mol,如果此时移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
|
| A. | 0.40mol | B. | 0.20mol |
|
| C. | 小于0.20mol | D. | 大于0.20mol,小于0.40mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图示意铁在氯气中燃烧的实验,铁丝点燃后,为维持燃烧继续,正确的操作是() 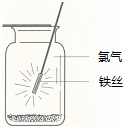
A. 铁丝应始终置于集气瓶瓶口位置
B. 迅速将铁丝插入集气瓶接近瓶底位置
C. 将铁丝从瓶口位置慢慢伸向瓶底位置
D. 铁丝应不断上下移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com