
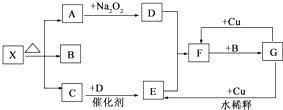
| ||
| △ |
| ||
| △ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定量的Fe与含1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
| B、1 mol AlCl3在熔融时离子总数为0.4NA |
| C、常温常压下,等质量的SO2、S2含有相同的分子数 |
| D、125 g CuSO4?5H2O晶体中含有0.5NA个Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
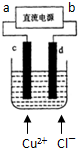
| A、a端是直流电源的负极 |
| B、通电使氯化铜发生电离 |
| C、阳极上发生的反应:Cu2++2e→Cu |
| D、通电一段时间,在阴极附近观察到有黄绿色气体产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com