
| 12.12��10-6mol |
| 30��10-3L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
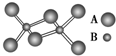 ij��������Ķ��۷��ӽṹ��ͼ���÷�����A��B����Ԫ�ض��ǵ������ڵ�Ԫ�أ�����������ԭ������㶼�ﵽ8�����ȶ��ṹ�����й��ڸû������˵������ȷ���ǣ�������
ij��������Ķ��۷��ӽṹ��ͼ���÷�����A��B����Ԫ�ض��ǵ������ڵ�Ԫ�أ�����������ԭ������㶼�ﵽ8�����ȶ��ṹ�����й��ڸû������˵������ȷ���ǣ�������| A����ѧʽ��Al2Cl6 |
| B�����������Ӽ��ͷǼ��Թ��ۼ� |
| C���ڹ�̬ʱ���γɵľ����Ƿ��Ӿ��� |
| D�������ӻ����������״̬���ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ɱ���CO2���壩����� |
| B��ɳ�� |
| C����ĭ����� |
| D��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��NH4+����c��Cl-����c��OH-����c��H+�� |
| B��c��Cl-����c��NH4+����c��OH-����c��H+�� |
| C��c��Cl-����c��NH4+����c��H+����c��OH-�� |
| D��c��NH4+��+c��H+���Tc��Cl-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ȼ�����Һ��Ӧ��Fe+Fe3+�T2Fe2+ |
| B���������廯����Һ��Ӧ��Cl2+2Br-�TBr2+2Cl- |
| C������������������Һ��Ӧ��H++OH-�TH20 |
| D��̼��������ᷴӦ��CO32-+2H+�TH2O+C02�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
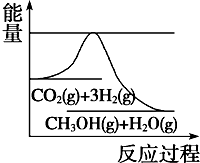 ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�| ʵ �� �� |
�� �� /�� |
��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
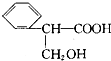 ������ѧ��Ӧ���ǣ�������
������ѧ��Ӧ���ǣ�������| A���٢� | B���ڢ� | C��ֻ�Т� | D���ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com