
| A. | 现象相同,生成Al(OH)3的量相同 | B. | 现象不同,生成Al(OH)3的量相同 | ||
| C. | 现象相同,生成Al(OH)3的量不同 | D. | 现象不同,生成Al(OH)3的量不同 |
分析 将NaOH溶液逐滴加入AlCl3溶液中,发生:Al3++3OH-═Al(OH)3↓,将AlCl3溶液逐滴加入NaOH溶液中,分别发生:Al3++4OH-=AlO2-+2H2O,Al3++3AlO2-+6H2O=4Al(OH)3↓,以此进行判断.
解答 解:350mL 1mol•L-1NaOH溶液中n(NaOH)=0.35mol,100mL 1mol•L-1的AlCl3溶液中n(AlCl3)=0.1mol,则
(1)将NaOH溶液逐滴加入AlCl3溶液中,发生:Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-=Al3++3H2O,现象为观察到白色沉淀,生成沉淀为0.1mol-0.05mol=0.05mol,
(2)将AlCl3溶液逐滴加入NaOH溶液中,分别发生:Al3++4OH-=AlO2-+2H2O,生成$\frac{0.35}{4}$molAlO2-,物质的量为0.0875mol,剩余铝离子物质的量=0.1mol-0.0875mol=0.0125mol,Al3++3AlO2-+6H2O=4Al(OH)3↓,铝离子过量,生成沉淀为0.05mol,先没有沉淀后出现沉淀,
所以二者现象不同,但沉淀质量相等.
故选B.
点评 本题考查的化合物的性质,题目难度不大,学习中注意相关基础知识的积累,特别是铝三角知识,为中学元素化合物中的重要内容.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:选择题
| A. | 亚氨基锂(Li2NH)中N的化合价为-1 | |
| B. | 此法储氢和钢瓶储氢的原理相同 | |
| C. | Li+和H-的半径相同 | |
| D. | 该反应中氢气既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
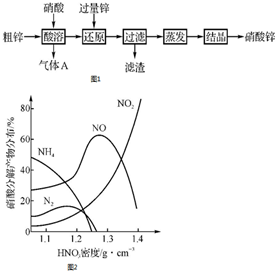 硝酸锌常用于工业电镀、媒染剂等,用粗锌[含少量Zn2(OH)2CO3、Fe和Cu]和硝酸为原料制备硝酸锌的实验流程如图1.活泼金属(如Zn、Fe、Mg等)与不同浓度HNO3溶液反应时主要还原产物不同.如图2是Fe与不同浓度HNO3溶液反应时的主要还原产物.
硝酸锌常用于工业电镀、媒染剂等,用粗锌[含少量Zn2(OH)2CO3、Fe和Cu]和硝酸为原料制备硝酸锌的实验流程如图1.活泼金属(如Zn、Fe、Mg等)与不同浓度HNO3溶液反应时主要还原产物不同.如图2是Fe与不同浓度HNO3溶液反应时的主要还原产物.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 得到碘酸钾晶体,你建议的方法是蒸发结晶.
得到碘酸钾晶体,你建议的方法是蒸发结晶.| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li2C2水解生成C2H4 | B. | Al4C3水解生成丙炔 | ||
| C. | Mg2C3水解生成丙烯 | D. | ZnC2水解生成C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数分别为176、177 | B. | 互称为同位素 | ||
| C. | 质量数均超过质子数的2倍 | D. | 是同一种核素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com