
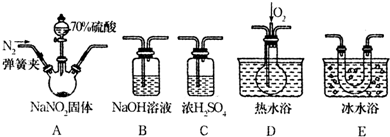
���� ��1�����������������Ʒ�Ӧ��������ijɷ�ΪNO��NO2������NO������е�������������NO2������ʵ�鿪ʼǰҪ��װ���еĿ����ž������ݸ�����װ�õ����ÿ�֪��C����ˮ������Bβ����������ֹ��Ⱦ������D����NO��E��ȴ��������������D����NO��
����ɫ��NO��������Ӧ���ɺ���ɫ�Ķ����������ݴ˿��ж�NO�IJ�����
��װ��A��Ϊ�������������Ʒ�Ӧ���������ơ�NO��NO2��ˮ��
��Cװ����Ҫ�����Ǹ��������壬�����ˮ������������ˮ��Ӧ����һ���������ݴ˴��⣻
��2������������Һ�У�����AgNO3��AgCl��AgNO2���ܽ�ƽ�������ƶ������DZ�����Һ��AgNO2���ܽ�ȸ�С��������Һ��AgCl�����϶ࣻ
��3��֤��HNO2��������������ˮ��ʼ��Ի���������ȫ����ⶨ������Һ��pHֵ�ȣ�
��� �⣺��1�����������������Ʒ�Ӧ��������ijɷ�ΪNO��NO2������NO������е�������������NO2������ʵ�鿪ʼǰҪ��װ���еĿ����ž�����Ӧǰͨ�뵪����Ŀ�����ž�װ���ڵĿ�������ֹ���ܲ�����NO��������NO2����ɶ�A�з�Ӧ�������ĸ��ţ����ݸ�����װ�õ����ÿ�֪��C����ˮ������Bβ����������ֹ��Ⱦ������D����NO��E��ȴ��������������D����NO����������������˳��ΪA��C��E��D��B��
�ʴ�Ϊ���ž�װ���ڵĿ�������ֹ���ܲ�����NO��������NO2����ɶ�A�з�Ӧ�������ĸ��ţ�C��E��D��
����ɫ��NO��������Ӧ���ɺ���ɫ�Ķ�������������ȷ��A�в��������庬��NO�����ݵ�������װ��D��ͨ�����������ֺ���ɫ���壬
�ʴ�Ϊ��װ��D��ͨ�����������ֺ���ɫ���壻
��װ��A��Ϊ�������������Ʒ�Ӧ���������ơ�NO��NO2��ˮ����Ӧ����ʽΪ2NaNO2+H2SO4=Na2SO4+NO��+NO2��+H2O��
�ʴ�Ϊ��2NaNO2+H2SO4=Na2SO4+NO��+NO2��+H2O��
��Cװ����Ҫ�����Ǹ��������壬�����ˮ������������ˮ��Ӧ����һ���������������û��װ��C��ˮ��������NO2��Ӧ����NO����ɶ�NO����Դ��ʶ���壬
�ʴ�Ϊ��ˮ��������NO2��Ӧ����NO����ɶ�NO����Դ��ʶ���壻
��2����AgCl��AgNO2��������Һ�У�ǰ��c��Ag+�����ں���c��Ag+����c��Cl-����c��NO2-��������AgCl��AgBr��������Һ���ʱ������������ת�������ɸ����C���������ͬʱ����Һ��n��Cl-����ԭ��AgCl������Һ�д�����������ŨAgNO3��Һʱ��AgNO2�����������࣬��AgCl�������Ӹ��࣬
�ʴ�Ϊ�����ڣ�
��3��֤��HNO2������ķ����в�NaNO2��Һ��pH�����0.1mol/L HNO2��Һ��pH�ȣ�
�ʴ�Ϊ����NaNO2��Һ��pH�����0.1mol/L HNO2��Һ��pH�ȣ�
���� ���⿼����ʵ�鷽����ơ����ʵļ��顢���ܵ���ʵ��ܽ�ƽ�⣬Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��Ŀ�Ѷ��еȣ������ʱע��AgNO2���ܽ�ȱ�AgCl�����������������ܽ�ƽ�������ƶ������ɳ������࣬��Ŀ�Ѷ��еȣ�


 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
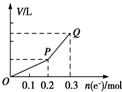 �ö��Ե缫�������ͭ��Һ����������ת�Ƶ��ӵ����ʵ������������������Ĺ�ϵ��ͼ��ʾ���������������ͬ״���²ⶨ������ʹ��Һ�ָ�����ʼ״̬��������Һ�м��루������
�ö��Ե缫�������ͭ��Һ����������ת�Ƶ��ӵ����ʵ������������������Ĺ�ϵ��ͼ��ʾ���������������ͬ״���²ⶨ������ʹ��Һ�ָ�����ʼ״̬��������Һ�м��루������| A�� | 0.1mol CuO | B�� | 0.1 mol CuCO3 | ||
| C�� | 0.1mol Cu��OH��2 | D�� | 0.05 mol Cu2��OH��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
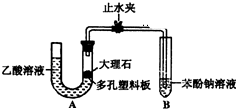 ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮̽�����ᡢ̼��ͱ��ӵ�����ǿ����ϵ��Уѧ���������ͼ��ʵ��װ�ã��г���������ȥ����
ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮̽�����ᡢ̼��ͱ��ӵ�����ǿ����ϵ��Уѧ���������ͼ��ʵ��װ�ã��г���������ȥ���� -ONa��Һ��pH����pH�ɴ�С���е�˳��Ϊbdac��������Һ��ţ�
-ONa��Һ��pH����pH�ɴ�С���е�˳��Ϊbdac��������Һ��ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
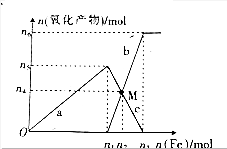 ��������۵����ʵ����Ĺ�ϵ��ͼ��ʾ��
��������۵����ʵ����Ĺ�ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
��| ʵ������ | ԭ�� |
| ��Һ�������ɫ��Ϊ��ɫ | ������ˮ��Ӧ���ɵ�H+ʹʯ���ɫ |
| �����Һ��Ϊ��ɫ | _������ˮ��Ӧ���ɵ�HClO��ʯ������Ϊ��ɫ���� |
| Ȼ����Һ����ɫ��Ϊdz����ɫ | ����ͨ�����������ˮʹ��Һ��dz����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CO��H2��Ϊ��Ҫ��ȼ�Ϻͻ���ԭ�ϣ�����ʮ�ֹ㷺��Ӧ�ã�
CO��H2��Ϊ��Ҫ��ȼ�Ϻͻ���ԭ�ϣ�����ʮ�ֹ㷺��Ӧ�ã��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com