
| A. | 沙里淘金,利用了沙子和金子的密度不同 | |
| B. | 海水晒盐,利用了水和NaCl的沸点不同 | |
| C. | 酒糟酿酒,利用了粮食和酒精分子的颗粒大小不同 | |
| D. | 植物油能萃取蔬菜汁中的植物精华--维生素,利用了维生素在水和油中溶解度不同 |
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钾与硝酸反应 | B. | 焦炭在高温下与水蒸气反应 | ||
| C. | 石灰石分解成氧化钙和二氧化碳 | D. | Ba(OH)2•8H2O与NH4Cl的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
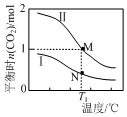 两个容积均为2L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g),起始物质的量见表.实验测得两容器不同温度下达到平衡时CO2的物质的量如图所示,下列说法正确的是( )
两个容积均为2L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g),起始物质的量见表.实验测得两容器不同温度下达到平衡时CO2的物质的量如图所示,下列说法正确的是( )| 容器 | 起始物质的量 | |
| NO | CO | |
| Ⅰ | 1 mol | 3 mol |
| Ⅱ | 6 mol | 2 mol |
| A. | N点的平衡常数为0.04 | |
| B. | M、N两点容器内的压强:P(M)>2P(N) | |
| C. | 若将容器Ⅰ的容积改为1 L,T1温度下达到平衡时c(CO2)=0.25 mol•L-1 | |
| D. | 若将容器Ⅱ改为绝热容器,实验起始温度为T1,达平衡时NO的转化率小于16.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
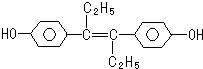
| A. | 可与NaOH和NaHCO3发生反应 | |
| B. | 它易溶于有机溶剂 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,至少8个碳原子一定共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 回收废电池外壳的金属材料 | |
| B. | 防止废电池中的汞、镉和铅等重金属离子对土壤和水源的污染 | |
| C. | 不使电池中渗漏的电解液腐蚀其他物品 | |
| D. | 提炼稀有金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动 | B. | x+y=z | ||
| C. | C的体积分数升高 | D. | B的转化率降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com