
【题目】英国科学家道尔顿曾经说过:“有的人能够远远超越其他人,其主要原因与其说是天才,不如说他有专心致志坚持学习和不达目的决不罢休的顽强精神”,道尔顿为近代化学科学的发展作出的卓越贡献是( )
A. 提出元素的概念
B. 建立燃烧现象的氧化学说
C. 提出原子学说,为近代化学的发展奠定坚实的基础
D. 发现元素周期律,把化学元素及其化合物纳入一个统一的体系
科目:高中化学 来源: 题型:
【题目】下列实验操作或事实与预期实验目的或所得结论对应正确的是( )
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含所有FeCl3 |
B | CaO | 用生石灰制备NaOH溶液 |
C | 足量过氧化钠投入酚酞溶液后,溶液先变红,最后呈无色 | 过氧化钠与酚酞溶液不反应 |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究钠及其化合物有重要意义。
(1)实验室配制0.1molL-1的碳酸钠溶液480mL,根据配制溶液的过程,回答问题:
①实验中除需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的其他玻璃仪器是_________。
②实验中需用托盘天平(带砝码)称量碳酸钠固体_______________g。
③某同学配制 Na2CO3溶液的过程如图所示。你认为该同学的错误有___________。
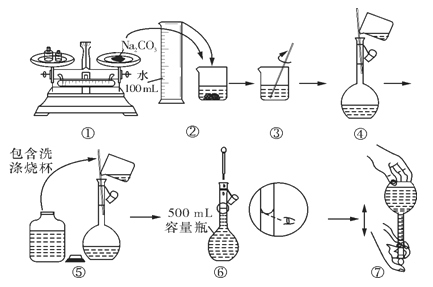
A.①⑥ B.②④⑦ C.①⑤⑥ D.⑤⑥⑦
④下列实验操作会使配得的溶液浓度偏小的是___________。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.容量瓶使用前没有经过干燥,瓶中有少量的水
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
(2)过氧化钠保存不当容易变质生成Na2CO3。某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液和水,证明过氧化钠已经部分变质:_________________(说明操作、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电离常数的说法正确的是( )
A.电离常数随着弱电解质的浓度增大而增大
B.CH3COOH的电离常数表达式为Ka= ![]()
C.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
D.电离常数只与温度有关,与浓度无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2![]() CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
A. 反应①中CS2作氧化剂
B. 反应①中每生成1mol S2Cl2转移4mol电子
C. 反应②中氧化产物与还原产物的物质的量之比为3:1
D. 反应②中S2Cl2既作氧化剂又作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 含有不同种元素的纯净物叫做化合物 B. 盐中一定含有金属元素
C. 水溶液中能电离出H+的化合物一定是酸 D. 含有氧元素的化合物一定是氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电离常数的说法正确的是( )
A.电离常数随着弱电解质的浓度增大而增大
B.CH3COOH的电离常数表达式为Ka= ![]()
C.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
D.电离常数只与温度有关,与浓度无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka(CH3COOH)=Kb(NH3H2O)=1.75×10﹣5 , 下列说法正确的是( )
A.用0.1molL﹣1的盐酸滴定0.1molL﹣1的氨水时,可用酚酞作指示剂
B.0.2 molL﹣1的醋酸与0.1 molL﹣1的氢氧化钠溶液等体积混合,所得溶液中:c(CH3COO﹣)+c(OH﹣)=C(CH3COOH)+C(H+)
C.pH=3的醋酸与pH=11的氨水等体积混合,所得溶液中有水电离出的C(H+)=1×10﹣7 molL﹣1
D.pH=3的盐酸与pH=11的氨水等体积混合,所得溶液中C(NH3H2O)>C(NH4+)>C(Cl﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com