
【题目】在下列各种情况下,电离方程式书写正确的是
A.熔融状态下的NaHSO4电离:NaHSO4===Na++H++SO![]()
B.H2CO3的电离:H2CO3![]() 2H++CO
2H++CO![]()
C.Fe(OH)3的电离:Fe(OH)3===Fe3++3OH-
D.水溶液中的NaHSO3电离:NaHSO3===Na++HSO![]()
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。
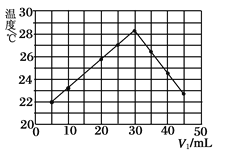
下列叙述正确的是
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中肯定为纯净物的是
A. 只由一种元素组成的物质
B. 只由一种原子组成的物质
C. 只由一种分子组成的物质
D. 只由一种元素的阳离子与另一种元素的阴离子组成的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 分子式为C5H10O2的羧酸共有3种
B. 分子式为C3H9N的异构体共有4个
C. 某烷烃CnH2n+2的一个分予中,含有共价键的数目是3n+1
D. 某烷烃CnH2n+2的一个分子中,含有非极性键的数目是n-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为周期表中前四周期的元素。请按要求回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
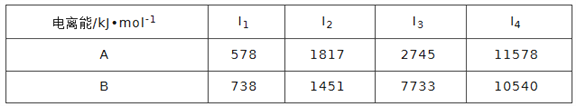
下列有关A、B的叙述不正确的是(____)a.离子半径A<B b.电负性A<B
c.单质的熔点A>B d.A、B的单质均能与氧化物发生置换
e.A的氧化物具有两性 f.A、B均能与氯元素构成离子晶体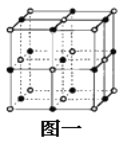
(2)C是地壳中含量最高的元素,C基态原子的电子排布式为_______。Cn-比D2+少l个电子层。二者构成的晶体的结构与NaCl晶体结构相似(如图一所示),晶体中一个D2+周围和它最邻近且等距离的D2+有_____个。
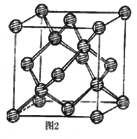
(3)E元素原子的最外层电子数是其次外层电子数的2倍,则乙酸分子中E原子的杂化方式有_____。E的一种单质其有空间网状结构,晶胞结构如图2。己知位于晶胞内部的4个原子,均位于体对角线的1/4或3/4处,E-E键长为apm,则E晶体的密度为_________g/cm3(用含有NA、a的式子表示)。
(4)F与硒元素同周期,F位于p区中未成对电子最多的元素族中,F的价电子排布图为
______,FO33-离子的空间构型为__________;F第一电离能_______硒元素(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4===2H++SO![]()
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com