
【题目】已知在葡萄糖溶液中有一种环状结构的葡萄糖分子(分子式C6H12O6),且有下列平衡关系:
(1)这种环状结构的分子是通过链式葡萄糖分子中的__________基和___________基通过_______________________反应而形成的。
(2)用(1)反应方式写出由两种简单的有机物合成某一链状醇醚(如右)的反应方程式:________
![]()
(3)已知溴水(Br2+H2O)可以将多羟基醛基氧化成羧基。写出溴水与葡萄糖反应的化学方程式_________________________________________
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A. 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA
B. 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA
C. 标准状况下,44.8L NO与22.4 L O2反应后的分子数是2NA
D. 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别方法不可行的是
A. 用新制的氯氧化铜悬浊液可以鉴别甲醇、乙醛、乙酸
B. 用溴水鉴别苯,丙烯、四氯化碳
C. 用点燃的方法可以鉴别乙烯、乙炔、苯
D. 用NaOH溶液鉴别溴乙烷,甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E~N等元素在周期表中的相对位置如下表。E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是

A.K的氢化物水溶液显碱性
B.F的单质与氧气反应只生成一种氧化物
C.H与N的原子核外电子数相差14
D.最高价氧化物的水化物酸性:K > L > M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷、乙烯、乙炔它们及其衍生物一氯乙烷、氯乙烯、乙醇、乙醛、乙酸、乙酸乙酯都有很重要的用途。
(1)乙炔在空气中燃烧的现象____________________________________________________
由乙烷制取一氯乙烷的反应条件___________________,由乙烯制取乙醇的反应类型_________
(2)一氯乙烷分子中的官能团为__________________。聚氯乙烯的结构简式为________________。
(3)写出由乙醛生成乙酸的化学反应方程式。__________________________________________
(4)写出乙酸的一种同分异构体的结构简式____________________________;检验该同分异构体是否含有醛基操作_________________________________________________________
______________________________________________________________
(5)乙二醇(HOCH2CH2OH)也是一种很重要的化工原料,请完成由一氯乙烷合成乙二醇的路线图(合成路线常用的表示方式为:![]() )
)
____________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制一定物质的量浓度的溶液,一定要用到的一组仪器是( )
A. 托盘天平、药匙、烧杯、容量瓶
B. 量筒(或滴定管、移液管)、容量瓶
C. 容量瓶、烧杯、玻璃棒、胶头滴管
D. 容量瓶、烧杯、玻璃棒、分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②:![]() (g)→
(g)→![]() (g)+H2(g),ΔH= +117.6kJ/mol
(g)+H2(g),ΔH= +117.6kJ/mol
②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式__________________。该反应的化学平衡常数K=_________(用K1、K2表示)。
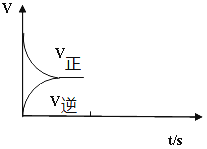
(2)温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。__________________
Ⅱ.一定条件下,合成氨反应为:如图表示在此反应过程中的能量的变化,如图表示在2L的密闭中反应时N2的物质的量随时间的变化曲线.如图表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
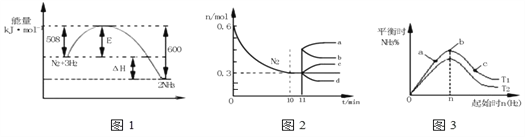
(3)由如图信息,计算10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为____(填“a”或“b”或“c”或“d”)
(4)如图a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是____点,温度T1____T2(填“>”或“=”或“<”)
Ⅲ.H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:
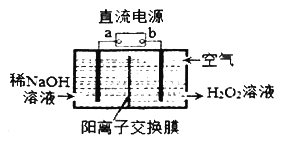
(5)a为______(正极、负极)
(6)通入空气的电极反应式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中盛有浓硫酸,B中盛有乙醇、无水醋酸钠、碎瓷片,D中盛有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl26C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用是_______________________________________________;
(2)球形干燥管C的作用是_______________________。反应结束后D中的现象是________________________________________________________________________________;
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,除去_________;
再加入_______除水(填写选项字母),然后进行___________(填写操作名称),得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com