
| A. | 不慎将浓碱溶液沾到皮肤上,立即用大量硫酸冲洗,然后再用水冲洗 | |
| B. | 不慎将酸溅到眼中,立即用大量水冲洗,边洗边眨眼睛 | |
| C. | 实验时手指上不小心沾上浓硫酸,立即用NaOH溶液清洗 | |
| D. | 酒精不慎洒在实验桌上烧起来时,立即用水浇灭 |
科目:高中化学 来源: 题型:解答题
| 装置 | 现象 | 结论及解释 |
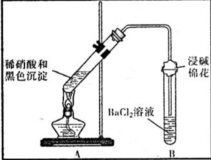 | ①A试管中黑色沉淀逐渐溶解 ②A试管上方出现红棕色气体 ③B试管中出现白色沉淀 | a.现象②说明褐色沉淀具有 还原性性. b.试管B中产生白色沉淀的总反应的离子方程式为 NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | TiCl4在反应I中是还原产物,在反应Ⅱ中是氧化剂 | |
| B. | C、Mg在反应中均为还原剂,被氧化 | |
| C. | 每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移1.6 mol e- | |
| D. | 反应I中b=c=2,反应II中Mg的还原性大于Ti |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Ba2+、Cl-、SO42- | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | Cl-、Na+、NO3-、Ca2+ | D. | Fe2+、NO3-、I-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
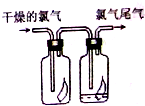 如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到右瓶的现象是:有色布条褪色,发生此现象的原因是Cl2+H2O?HCl+HClO.(用有关的方程式解释)
如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到右瓶的现象是:有色布条褪色,发生此现象的原因是Cl2+H2O?HCl+HClO.(用有关的方程式解释)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 化学式 | 熔点/℃ | 沸点/℃ | 密度/g.cm-3 | 在水中溶解度 |
| 甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | C4H8O2 | -84 | 88 | 0.90 | 可溶 |
| A. | 萃取 | B. | 蒸发 | C. | 蒸馏 | D. | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、HCO3- | B. | NH4+、Al3+、SO42- | C. | Na+、AlO2-、NO3- | D. | Cu2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
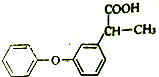 请按要求回答下列问题:
请按要求回答下列问题: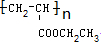 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
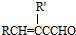 +H2O(R、R′表示烃基或氢),高分子化合物PVB的合成就是其一种重要应用.
+H2O(R、R′表示烃基或氢),高分子化合物PVB的合成就是其一种重要应用.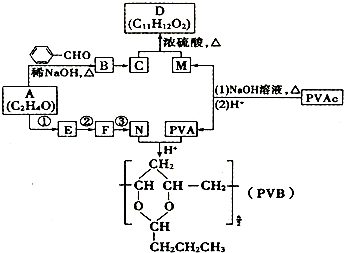

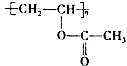
 合成B的化学方程式是
合成B的化学方程式是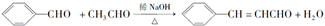 .
.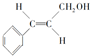 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com