
| A. | Li在空气中的燃烧产物为Li2O2 | B. | Be(OH)2 溶于NaOH可生成BeO2- | ||
| C. | BeO是两性氧化物 | D. | B2O3既能溶于强酸又能溶于强碱 |
分析 元素周期表中,处于对角线位置的元素具有相似的性质,则根据Mg、Al、Si及其化合物的性质可推断BeO、Be(OH)2的性质,根据Si的性质推断B可能具有的性质.
解答 解:A.Mg燃烧生成MgO,则由对角线规则可知,Li在空气中的燃烧产物为Li2O,故A错误;
B.Al(OH)3与NaOH反应生成AlO2-,则由对角线规则可知,Be(OH)2 溶于NaOH可生成BeO22-,故B错误;
C.Be与Al处于对角线位置,性质相似,已知Al2O3为两性氧化物,则BeO为两性氧化物,故C正确;
D.B和Si处于对角线位置,性质相似,SiO2不溶于强酸,则B2O3也不溶于强酸,故D错误;
故选C.
点评 本题考查元素周期表和周期律的关系,为高频考点,注意对角线原则,把握常见元素化合物的性质,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加体系的压强 | B. | 减少C的物质的量浓度 | ||
| C. | 增加A的物质的量 | D. | 升高体系的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl水溶液的导电性很弱,所以AgCl是弱电解质 | |
| B. | 所有盐类都能促进水的电离 | |
| C. | 碳酸钠溶液加水稀释过程中,溶液中各离子浓度都减小 | |
| D. | 将1 mL pH=3的HX溶液稀释到10 mL,若溶液的pH<4,则HX为弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在自然界中以化合态的形式存在 | B. | 单质常用作半导体材料和光导纤维 | ||
| C. | 最高价氧化物不与任何酸反应 | D. | 气态氢化物比甲烷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
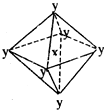 在某晶体中,与某一种微粒x距离最近且等距离的另一种微粒y所围成的空间构型为正八面体型(如图).该晶体可能为( )
在某晶体中,与某一种微粒x距离最近且等距离的另一种微粒y所围成的空间构型为正八面体型(如图).该晶体可能为( )| A. | NaCl | B. | CsCl | C. | CO2 | D. | SiO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com