
| A. | 在周期表金属与非金属区分界线附近找 | |
| B. | 在周期表左下方找 | |
| C. | 在周期表右上方找 | |
| D. | 在过渡元素中找 |
科目:高中化学 来源: 题型:选择题
| A. | 胶体的聚沉是化学变化 | |
| B. | 含有0.01mol FeCl3的溶液制成的胶体中,胶体粒子的数目约为6.02×1021个 | |
| C. | 胶体的介稳性与胶体粒子直径大小有关 | |
| D. | NaCl晶体既可制成溶液又可制成胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{Vρ}{22400}$mol•L-1 | B. | $\frac{V}{22.4}$mol•L-1 | ||
| C. | $\frac{Vρ}{22400+17V}$mol•L-1 | D. | $\frac{1000Vρ}{22400+17V}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第2周期元素从左到右,最高正化合价从+1递增到+7 | |
| B. | 在周期表中的过渡元素中寻找半导体材料 | |
| C. | 元素周期表中元素的性质与元素在周期表中的位置有关 | |
| D. | 同种元素的原子均有相同的质子数和中子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “PX”的化学式为C8H10,核磁共振氢谱图上有2组吸收峰 | |
| B. | “PX”能使酸性高锰酸钾溶液褪色,属于苯的同系物 | |
| C. | “PX”的一溴代物和二溴代物的同分异构体分别有1种、3种 | |
| D. | “PX”不溶于水,密度比水小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
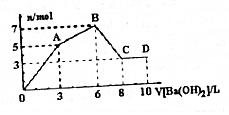 向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/LBa(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所所得沉淀的量的关系如图,下列说法不正确的是( )
向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/LBa(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所所得沉淀的量的关系如图,下列说法不正确的是( )| A. | 图中C点铝元素存在的形式是AlO2- | |
| B. | 原混合溶液中c[Al2(SO4)3]:c(AlCl3)=1:2 | |
| C. | 向D点溶液中通入过量CO2气体,最终将得到9mol沉淀 | |
| D. | OA段反应的离子方程式为:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
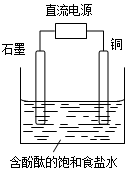
| A. | 石墨电极附近溶液呈红色 | B. | 铜电极上发生还原反应 | ||
| C. | 溶液中的Na+向石墨电极移动 | D. | 铜电极附近观察到黄绿色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com