
����Ŀ����ϩ��һ����Ҫ�Ļ���ԭ�ϣ���������Ϊԭ����ȡ����ش��������⣺
��1����ͳ�����ѽⷨ���ִ��������ѽⷨ���Ȼ�ѧ����ʽ���£�
C2H6(g)��C2H4(g)��H2(g) ��H1����136kJ��mol��1
C2H6(g)��![]() O2(g)��C2H4(g)��H2O(g) ��H2����110kJ��mol��1
O2(g)��C2H4(g)��H2O(g) ��H2����110kJ��mol��1
��֪ˮ��������ΪH2O(l)��H2O(g) ��H3����44kJ��mol��1
�ҷ�Ӧ��صIJ��ֻ�ѧ�������������£�
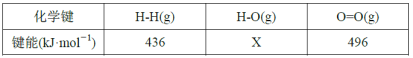
���ɴ˼���x��___��ͨ���Ƚ���H1����H2��˵�������ѽⷨ��ͨ��������������___��
������������ͬ�����������ѻ�������ϩ�ķ�Ӧ�У�ʵ������T1��P1��T2��P2�����¸÷�Ӧ��C2H6ƽ��ת������ͬ����T1��T2����P1___P2(������������������������)��
����������з�Ӧ�ķ�Ӧ�ȣ�C2H6(g)��![]() O2(g)��C2H4(g)��H2O(l) ��H3��___��
O2(g)��C2H4(g)��H2O(l) ��H3��___��
��2��һ�������£������Ϊ2L���ܱ������У�����1molC2H6������ͳ�ѽⷨ����ϩ��
��ij�¶��£�10min��÷�Ӧ��ƽ�⣬��ʱC2H6�����ʵ���Ũ��Ϊ0.2mol��L��1���ӷ�Ӧ��ʼ��ƽ�⣬��ϩ��ƽ����Ӧ����v(C2H4)��___��
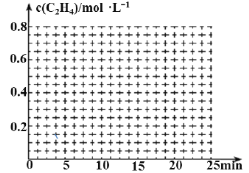
���������������������£�15minʱ������ϵ�¶ȣ�20min�ﵽ��ƽ�⣬�����±ߵ�����ϵ�л���0��25 min��c(C2H4)��ʱ��仯���ߣ�____��
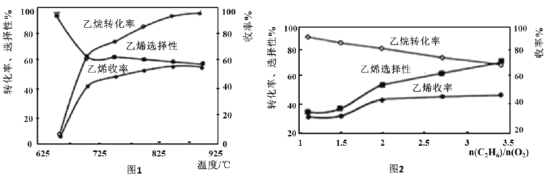
��3������������ѽⷴӦ�����г���C2H4�⣬������CH4��CO��CO2�ȸ�����(����Ӧ��Ϊ���ȷ�Ӧ)��ͼ1Ϊ�¶ȶ����������ѽⷴӦ���ܵ�Ӱ�졣�����ת�������¶ȵ����߶����ߵ�ԭ����___����Ӧ������¶�Ϊ___(��ѡ�����)��
A.700�� B.750�� C.850�� D.900��
[��ϩѡ���ԣ�![]() ����ϩ���ʣ�����ת���ʡ���ϩѡ����]
����ϩ���ʣ�����ת���ʡ���ϩѡ����]
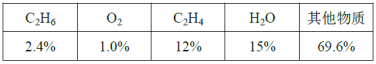
��4������������Ӧ�У����������ͻᵼ�·�Ӧ������̿��������Ӧ�ܡ�ͼ2Ϊn(C2H6)/n(O2)��ֵ�����������ѽⷴӦ���ܵ�Ӱ�졣�ж����������ѽ������![]() �����ֵ��___���жϵ�������___��
�����ֵ��___���жϵ�������___��
��5����ҵ�ϣ�������ϵ��ѹ�㶨Ϊ100kPa�������½��и÷�Ӧ��ͨ��������������Ļ�������в����������(����������������Ϊ70%)��������������Ŀ����___��
��6����Ӧ��ƽ��ʱ������ֵ�����������±���
������¶��µ�ƽ�ⳣ��Kp��___(��ƽ���ѹ����ƽ��Ũ�ȣ�ƽ���ѹ����ѹ���������)
���𰸡�465 ������Ӧʱ�ų�������Ϊ������Ӧ�ṩ��������Լ��Դ < ��154kJ��mol��1 0.03mol/(Lmin)  (˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ) ��Ȼ��Ӧ���ȣ�����Ӧδ��ƽ�⣬��ʱ�����¶ȣ���Ӧ���ʼӿ죬��Ӧ���ת�������� C 2 ��ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���� ����ӦΪ�������������ķ�Ӧ����ѹ����������壬�൱��������������������ͷ�ѹ��������ƽ�������ƶ�
(˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ) ��Ȼ��Ӧ���ȣ�����Ӧδ��ƽ�⣬��ʱ�����¶ȣ���Ӧ���ʼӿ죬��Ӧ���ת�������� C 2 ��ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���� ����ӦΪ�������������ķ�Ӧ����ѹ����������壬�൱��������������������ͷ�ѹ��������ƽ�������ƶ� ![]()
��������
��1����ͳ�����ѽⷨ���ִ��������ѽⷨ���Ȼ�ѧ����ʽ���£�
C2H6(g)��C2H4(g)��H2(g) ��H1����136kJ��mol��1 ��
C2H6(g)��![]() O2(g)��C2H4(g)��H2O(g) ��H2����110kJ��mol��1 ��
O2(g)��C2H4(g)��H2O(g) ��H2����110kJ��mol��1 ��
��֪ˮ��������ΪH2O(l)��H2O(g) ��H3����44kJ��mol��1 ��
�ҷ�Ӧ��صIJ��ֻ�ѧ�������������£�

�ټ���xǰ�����ȿ��������ݣ�Ԥ��Ӧͨ����֪��Ӧ�����H2(g)+![]() O2(g)��H2O(g)����H��Ȼ�����ü��ܽ��м��㡣ͨ���١��������Ȼ�ѧ����ʽ�ıȽϿ��Կ�����ͨ��O2�൱����H2��Ӧ����H2O����ų��������Ӷ�˵�������ѽⷨ��ͨ��������������Ϊ��Ӧ�ṩ������
O2(g)��H2O(g)����H��Ȼ�����ü��ܽ��м��㡣ͨ���١��������Ȼ�ѧ����ʽ�ıȽϿ��Կ�����ͨ��O2�൱����H2��Ӧ����H2O����ų��������Ӷ�˵�������ѽⷨ��ͨ��������������Ϊ��Ӧ�ṩ������
������������ͬ�����������ѻ�������ϩ�ķ�Ӧ�У�ʵ������T1��P1��T2��P2�����¸÷�Ӧ��C2H6ƽ��ת������ͬ����T1��T2��ƽ�������ƶ�����ı�ѹǿ��ƽ��Ӧ�����ƶ����ɷ�Ӧǰ������ķ�������ϵ����ȷ��Ϊʹƽ�������ƶ���P1��P2�Ĺ�ϵ��
�����ø�˹���ɣ������ڡ���������Ӧ����������з�Ӧ�ķ�Ӧ�ȣ�C2H6(g)��![]() O2(g)��C2H4(g)��H2O(l) ��H3��
O2(g)��C2H4(g)��H2O(l) ��H3��
��2���ٴӷ�Ӧ��ʼ��ƽ�⣬C2H6�����ʵ���Ũ�ȱ仯��Ϊ0.3mol��L��1��������ѧ����ʽ�������C2H4�����ʵ���Ũ�ȱ仯��Ϊ0.3mol��L��1���Ӷ������ϩ��ƽ����Ӧ����v(C2H4)��
����Ϊ����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���c(C2H4)������������ֵ��ֻ�ܵó�Ũ�ȷ�ΧΪ(0.3mol��L��1��0.5mol��L��1)�����ô˷���������ͼ��
��3�������ת�������¶ȵ����߶����ߵ�ԭ������Ȼ��Ӧ���ȣ�����Ӧδ��ƽ�⣬��ʱ�����¶ȣ���Ӧ���ʼӿ죬��Ӧ���ת��������Ӧ������¶�Ϊ850�棬��Ȼ�¶������ߣ���Ӧ���ת�������������Ⱥ�С������Ҫ���Ĵ��������ܣ��Ӿ����Ͽ��ǣ������㡣
��4�����������ѽ������![]() �����ֵ��2���жϵ������Ǵ�ʱ��ϩ�����ʻ����㶨��
�����ֵ��2���жϵ������Ǵ�ʱ��ϩ�����ʻ����㶨��![]() �����γɻ�̿��
�����γɻ�̿��
��5��������������Ŀ��������ӦΪ�������������ķ�Ӧ����ѹ����������壬�൱��������������������ͷ�ѹ��������ƽ�������ƶ���
��6�����¶��µ�ƽ�ⳣ������ʽΪ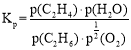 ������������ݣ��������Kp��
������������ݣ��������Kp��
��1��C2H6(g)��C2H4(g)��H2(g) ��H1����136kJ��mol��1 ��
C2H6(g)��![]() O2(g)��C2H4
O2(g)��C2H4
��֪ˮ��������ΪH2O(l)��H2O(g) ��H3����44kJ��mol��1 ��
�ҷ�Ӧ��صIJ��ֻ�ѧ�������������£�

�ٽ���-�ٵ�H2(g)+![]() O2(g)��H2O(g) ��H����246kJ��mol��1����H=436 kJ��mol��1+248 kJ��mol��1-2x=��246kJ��mol��1���Ӷ����x=465kJ��mol��1��ͨ���١��������Ȼ�ѧ����ʽ�ıȽϿ��Կ�����ͨ��O2�൱����H2��Ӧ����H2O����ų��������Ӷ�˵�������ѽⷨ��ͨ��������������������Ӧʱ�ų�������Ϊ������Ӧ�ṩ��������Լ��Դ����Ϊ��465��������Ӧʱ�ų�������Ϊ������Ӧ�ṩ��������Լ��Դ��
O2(g)��H2O(g) ��H����246kJ��mol��1����H=436 kJ��mol��1+248 kJ��mol��1-2x=��246kJ��mol��1���Ӷ����x=465kJ��mol��1��ͨ���١��������Ȼ�ѧ����ʽ�ıȽϿ��Կ�����ͨ��O2�൱����H2��Ӧ����H2O����ų��������Ӷ�˵�������ѽⷨ��ͨ��������������������Ӧʱ�ų�������Ϊ������Ӧ�ṩ��������Լ��Դ����Ϊ��465��������Ӧʱ�ų�������Ϊ������Ӧ�ṩ��������Լ��Դ��
����T1��T2��ƽ�������ƶ�����ı�ѹǿ��ƽ��Ӧ�����ƶ����ɷ�Ӧǰ����ķ������ȷ�Ӧ��С����ȷ��Ϊʹƽ�������ƶ������Сѹǿ���Ӷ��ó�P1<P2����Ϊ��<��
�����ø�˹���ɣ�����-�۵ã�C2H6(g)��![]() O2(g)��C2H4(g)��H2O(l) ��H3=��154kJ��mol��1����Ϊ����154kJ��mol��1��
O2(g)��C2H4(g)��H2O(l) ��H3=��154kJ��mol��1��������154kJ��mol��1��
��2���ٴӷ�Ӧ��ʼ��ƽ�⣬C2H6�����ʵ���Ũ�ȱ仯��Ϊ0.3mol��L��1��������ѧ����ʽ�������C2H4�����ʵ���Ũ�ȱ仯��Ϊ0.3mol��L��1���Ӷ������ϩ��ƽ����Ӧ����v(C2H4)=![]() ����Ϊ��0.03mol/(Lmin)��
������0.03mol/(Lmin)��
����Ϊ����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���c(C2H4)������������ֵ��ֻ�ܵó�Ũ�ȷ�ΧΪ(0.3mol��L��1��0.5mol��L��1)�����ô˷������ɵó���ͼ��
 (˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ)����Ϊ��
(˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ)����Ϊ�� (˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ)��
(˵����ͼ��ƽ��ʱ��c(C2H4)ֻҪ��0.3mol��L��1~0.5mol��L��1����ȷ)��
��3�������ת�������¶ȵ����߶����ߵ�ԭ������Ȼ��Ӧ���ȣ�����Ӧδ��ƽ�⣬��ʱ�����¶ȣ���Ӧ���ʼӿ죬��Ӧ���ת��������Ӧ������¶�Ϊ850�棬��Ȼ�¶������ߣ���Ӧ���ת�������������Ⱥ�С������Ҫ���Ĵ��������ܣ��Ӿ����Ͽ��ǣ������㡣��Ϊ����Ȼ��Ӧ���ȣ�����Ӧδ��ƽ�⣬��ʱ�����¶ȣ���Ӧ���ʼӿ죬��Ӧ���ת��������C��
��4�����������ѽ������![]() �����ֵ��2���жϵ������DZ�ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���١���Ϊ��2����ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���٣�
�����ֵ��2���жϵ������DZ�ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���١���Ϊ��2����ֵС��2ʱ����ϩ�����ʽϵͣ���ֵ����2ʱ����ϩ������������ٵ���������Ļ�̿��������Ӧ�ܣ�����ֵΪ2ʱ��ϩ���ʽϸߣ���Ӧ��̿���٣�
��5��������������Ŀ��������ӦΪ�������������ķ�Ӧ����ѹ����������壬�൱��������������������ͷ�ѹ��������ƽ�������ƶ�����Ϊ������ӦΪ�������������ķ�Ӧ����ѹ����������壬�൱��������������������ͷ�ѹ��������ƽ�������ƶ���
��6�����¶��µ�ƽ�ⳣ������ʽΪ ����Ϊ��
������![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 mol H��H���ļ�����436kJ��1 mol I��I���ļ�����151kJ��1 mol H��I���ļ�����299kJ����Է�ӦH2��g��+I2��g��![]() 2HI��g����˵��������ȷ���� �� ��
2HI��g����˵��������ȷ���� �� ��
A.���ȷ�ӦB.���ȷ�ӦC.���Ϸ�ӦD.���淴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ�����г��Բ�����![]() Ϊ��Һ��ͨ��������ԭ�ζ����ⶨ���������Һ��Ũ�ȣ��䷴Ӧ�Ļ�ѧ����ʽΪ��
Ϊ��Һ��ͨ��������ԭ�ζ����ⶨ���������Һ��Ũ�ȣ��䷴Ӧ�Ļ�ѧ����ʽΪ��![]() �����йز����Ƶζ��������ʵ�����������ȷ����( )
�����йز����Ƶζ��������ʵ�����������ȷ����( )
A.�ζ������У�������ر������������Ʊ���ԭ
B.�ü�ʽ�ζ�����ȡ���������Һ
C.�÷�Ӧ�У����ĵIJ������������ص����ʵ���֮��Ϊ5��2
D.Ϊ���ڵζ��յ���жϣ��ζ�ʱ��������ϵ�м���ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ý�������ʵ��,�ܵó���Ӧʵ����۵���(����)
ѡ�� | �� | �� | �� | ʵ����� |
|
A | Ũ���� | MnO2 | NaBr��Һ | ������Cl2>Br2 | |
B | Ũ��ˮ | ��ʯ�� | AgNO3��Һ | AgOH�������� | |
C | Ũ���� | Na2SO3 | FeCl3��Һ | SO2���л�ԭ�� | |
D | ϡ���� | Na2CO3 | Na2SiO3��Һ | �ǽ����ԣ�Cl>C>Si |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���к���NO2��NO��CO���к����壬��ȡ��״����22.4 L����β�����о����ָ�����ͨ����ת���������������к�����ɱ���ȫת��Ϊ����N2��CO2����ȡ�����β��ͨ��0.1 mol/L 50 mL NaOH��Һ�У����е�NO2��NOǡ�ñ���ȫ���ա���β����CO�������������Ϊ(˵��������β���������ɷ�������CO��NaOH��Һ������Ӧ)(����)
A. 0.4% B. 0.8% C. 2% D. 4%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼ѭ��������������ҵĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2����Ϊ��ѧ���о�����Ҫ���⡣
(1)����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g)![]() CO2(g)��H2(g)���õ������������ݣ�
CO2(g)��H2(g)���õ������������ݣ�
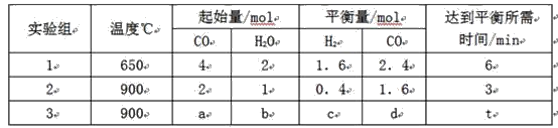
��ʵ��2������ƽ�ⳣ��K=______________��
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a/b ��ֵ_______(�����ֵ��ȡֵ��Χ)��
��ʵ��4����900��ʱ���ڴ������м���CO��H2O��CO2��H2��Ϊ1mol�����ʱv��_________v��(����<������>������=��)��
(2)��֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H����1275.6 kJ��mol
��2CO (g)+ O2(g) �� 2CO2(g) ��H����566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H����44.0 kJ��mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��____________
(3)��֪������һ�ֶ�Ԫ���ᣬ��������(NaHC2O4)��Һ�����ԡ������£���10 mL 0.01 mol��L-1H2C2O4��Һ�еμ�10mL 0.01mol��L-1NaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵ_____________��
(4)CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L �������ɳ�������CaCl2��Һ����СŨ��Ϊ_______________mol/L��
(5)�Զ�����(CH3OCH3)��������H2SO4Ϊԭ�ϣ���Ϊ�缫�ɹ���ȼ�ϵ�أ��乤��ԭ�������ȼ�ϵ�ص�ԭ�����ơ���д���õ�ظ����ϵĵ缫��Ӧʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���25 mL 0.1 mol��L��1NaOH��Һ����μ���0.2 mol��L��1CH3COOH��Һ��pH��μ�CH3COOH��Һ����Ĺ�ϵ��������ͼ��ʾ������������Һ���ʱ������仯�������й�����Ũ�ȹ�ϵ��˵���������(����)

A. ��A��B����һ�㣬��Һ��һ����c(Na��)��c(H��)��c(CH3COO��)��c(OH��)
B. ��B�㣺a>12.5������c(Na��)��c(CH3COO��)>c(OH��)��c(H��)
C. ��C�㣺c(Na��)>c(CH3COO��)>c(H��)>c(OH��)
D. ��D�㣺c(CH3COO��)��c(CH3COOH)��0.1mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��11��Ũ�Ⱦ�Ϊ ![]() ��
��![]() ��
�� ![]() ����һ�������·�����Ӧ
����һ�������·�����Ӧ![]()
![]()
![]() �����
�����![]() ��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
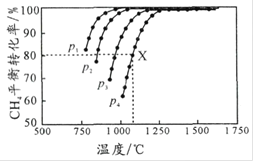
A.ƽ��ʱCO��![]() �����ʵ�����Ϊ
�����ʵ�����Ϊ![]()
B.![]() �ɴ�С��˳��Ϊ
�ɴ�С��˳��Ϊ ![]()
C.![]() �� p
�� p![]() �����£��÷�Ӧ
�����£��÷�Ӧ![]() ʱ�ﵽƽ���X����
ʱ�ﵽƽ���X���� ![]()
D.�����¶����ߣ��÷�Ӧ��ƽ�ⳣ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������£�����������Һ����0.1 mol/L NH4Cl��Һ����0.1 mol/L CH3COONH4��Һ����0.1 mol/L NH4HSO4��Һ����0.1 mol/L ��ˮ�������Ҫ����д���пհף�
��1����Һ����______�ԣ�������������������������������ԭ����___________�������ӷ���ʽ��ʾ����
��2�������£������Һ����pH=7����CH3COO����NH4+Ũ�ȵĴ�С��ϵ��c(CH3COO��) ________c(NH4+)������>������<������=������
��3�������£�0.1 mol/ L CH3COOH��Һ��ˮϡ�����У����б���ʽ����ֵ������____________������ĸ����
A��c(H+) B��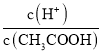 C��c(H+)��c(OH��) D��
C��c(H+)��c(OH��) D��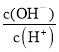 E��
E��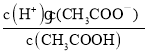
��4��25��ʱ����pH=9��NaOH��Һ��pH=4��H2SO4��Һ��ϣ������û����Һ��pH=7����NaOH��Һ��H2SO4��Һ�������Ϊ____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com