
| n(SO3²﹣):n(HSO3﹣) | 91 :9 | 1 :1 | 1 :91 |
| pH | 8.2 | 7.2 | 6.2 |
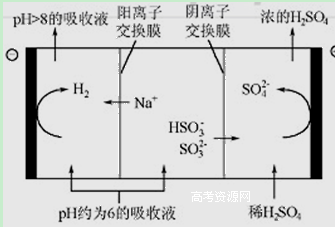


科目:高中化学 来源:不详 题型:单选题
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4×10-7 |
| K2=6×10-11 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应过程中,两个烧杯中产生氢气的速率一直相等 |
| B.反应结束后,两个烧杯中产生氢气的物质的量相等 |
| C.反应结束后,乙烧杯中有镁粉剩余 |
| D.反应结束后,甲烧杯中溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K> Kw | B.K= Kw | C.K< Kw | D.无法比较 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
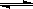 H+﹢OH-,△H>0,下列叙述不正确的是
H+﹢OH-,△H>0,下列叙述不正确的是| A.将水加热,pH减小 |
| B.恒温下,向水中加入少量固体KOH,Kw不变 |
| C.向水中滴入稀醋酸,c(H+)增大 |
| D.向水中加入少量固体NaClO,平衡逆向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 |
| B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
| C.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |
| D.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用湿润的pH试纸测定两种溶液的pH时,氨水的误差更大 |
| B.若混合后溶液恰好呈中性时:c(Cl-)= c(NH4+)+ c(NH3·H2O) |
| C.两溶液等体积混合时,充分反应后:c(Cl-)> c(NH4+)> c(OH-)> c(H+) |
| D.恰好反应呈中性时,所需氨水的体积大于盐酸的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲酸溶液中有大量的HCOOH分子和H+、HCOO— |
| B.甲酸能与水以任意比例互溶 |
| C.10mL 1 mol/L甲酸恰好与10mL 1 mol/LNaOH溶液完全反应 |
| D.在相同温度下,相同浓度的甲酸溶液的导电性比盐酸弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com