
| A. | 反应Z2+2A2+═2A3++2Z-不能进行 | |
| B. | Z元素在①③反应中均被氧化 | |
| C. | 氧化性由弱到强的顺序是XO${\;}_{4}^{-}$、Z2、B2、A3+ | |
| D. | 还原性由强到弱的顺序是A2+、B-、Z-、X2+ |
分析 A、氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性;
B、化合价升高的元素在反应中被氧化;
C、氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性;
D、氧化还原反应中,还原剂的还原性强于还原产物的还原性.
解答 解:A、根据反应2A2++B2=2A3-+2B-,可得氧化性是B2>A3+,2B-+Z2=B2+2Z-,可得氧化性是Z2>B2>A3+,反应Z2+2A2+=2A3++2Z-可以进行,故A错误;
B、Z元素在③中化合价降低,在反应中被还原,故B错误;
C、氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,:反应①16H++10Z-+2XO4-=2X2++5Z2+8H2O中,氧化性XO4->Z2;反应②2A2++B2=2A3-+2B-中,氧化性B2>A3+;反应③2B-+Z2=B2+2Z-中,氧化性Z2>B2,所以氧化性由强到弱的顺序是XO4->Z2>B2>A3+,故C错误;
D、氧化还原反应中,还原剂的还原性强于还原产物的还原性,反应①16H++10Z-+2XO4-=2X2++5Z2+8H2O中,还原性Z->X2+;反应②2A2++B2=2A3-+2B-中,还原性A2+>B-;反应③2B-+Z2=B2+2Z-中,还原性B->Z-,所以还原性由强到弱的顺序是A2+>B->Z->X2+,故D正确.
故选D.
点评 本题考查学生氧化还原反应中氧化性和还原性强弱判断规律:氧化还原反应中还原剂的还原性强于还原产物的还原性,氧化剂的氧化性强于氧化产物的氧化性.


科目:高中化学 来源: 题型:选择题
| A. | 50% | B. | 60% | C. | 80% | D. | 90% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用瓷坩埚熔融氢氧化钠或碳酸钠 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH | |
| C. | 读取量筒内液体的体积,俯视读数导致读数偏大 | |
| D. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(CH3COOH) | B. | C(H+) | C. | C(H+)/C(CH3COOH) | D. | C(CH3COOH)/C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
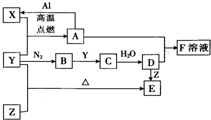 已知X、Y、Z为单质,其它为化合物.其中Y为气体,F溶液呈黄色,E是常见的温室气体,它们之间存在如下的转化关系(部分产物已经略去).请回答下列问题:
已知X、Y、Z为单质,其它为化合物.其中Y为气体,F溶液呈黄色,E是常见的温室气体,它们之间存在如下的转化关系(部分产物已经略去).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制乙烯和实验室制乙炔 | |
| B. | 乙烯使酸性高锰酸钾溶液褪色和乙醛使溴水褪色 | |
| C. | 苯酚制三溴苯酚和乙醛制乙醇 | |
| D. | 乙酸乙酯的水解和乙烯制聚乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 百分组成 NH3%=N2% | B. | 气体的密度不变 | ||
| C. | 压强不变 | D. | c(H2):c(N2):c(NH3)=3:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com