
|
下列实验Ⅰ~Ⅳ中,正确的是
| |
| [ ] | |
A. |
实验Ⅰ:配制一定物质的量浓度的溶液 |
B. |
实验Ⅱ:除去Cl2中的HCl |
C. |
实验Ⅲ:用水吸收NH3 |
D. |
实验Ⅳ:制备乙酸乙酯 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
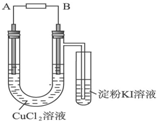 某学生用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,装置如图所示.
某学生用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,装置如图所示.| 64It |
| 2m×1.6×10-19 |
| 64It |
| 2m×1.6×10-19 |
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列实验事实所引出的相应结论正确的是
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com