
| A�� | B������������Ӧ��ˮ��������Ա�Eǿ | |
| B�� | ij������ɫ��Ӧ�ʻ�ɫ��������һ���Ǻ�C���� | |
| C�� | ��D�������ˮ��Ӧ�����Һ�еμӷ�̪����Һ��� | |
| D�� | B���⻯��ķе�һ������A���⻯�� |
���� ������Ԫ��A��B��C��D��E��ԭ��������������A��һ�ֺ����ڿ���ʱ����������һЩ������������A��̼Ԫ�أ�B���⻯���ˮ��Һ�ʼ��ԣ���BΪNԪ�أ�C��DΪ����Ԫ�أ�ԭ���������ڵ������ڵ������ڣ���Dԭ������������������K���������������������Ϊ2������DΪMgԪ�أ�CΪNaԪ�أ�����E���ʵ�ˮ��Һ�еμ�������ɫʯ����Һ���ܹ۲쵽�ȱ�����ɫ��������E��ClԪ�أ�
��� �⣺������Ԫ��A��B��C��D��E��ԭ��������������A��һ�ֺ����ڿ���ʱ����������һЩ������������A��̼Ԫ�أ�B���⻯���ˮ��Һ�ʼ��ԣ���BΪNԪ�أ�C��DΪ����Ԫ�أ�ԭ���������ڵ������ڵ������ڣ���Dԭ������������������K���������������������Ϊ2������DΪMgԪ�أ�CΪNaԪ�أ�����E���ʵ�ˮ��Һ�еμ�������ɫʯ����Һ���ܹ۲쵽�ȱ�����ɫ��������E��ClԪ�أ�
A������������Ա������ǿ����A����
B��ij������ɫ��Ӧ�ʻ�ɫ�������ʺ���NaԪ�أ������Ǻ����Σ�Ҳ����ΪNaOH�ȣ���B����
C��Mg�������ˮ��Ӧ������������þ����Һ�ʼ��ԣ��μӷ�̪����Һ��죬��C��ȷ��
D��A���⻯���Ǽ��顢B���⻯���ǰ�������������֮���γ�������е���ڼ���ģ���D����
��ѡ��C��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ������ض�Ԫ�ػ�����֪ʶ�Ŀ��飬Bѡ��Ϊ�״��㣬ע��������������ʵ�Ӱ�죮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
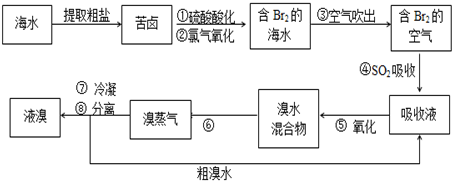
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
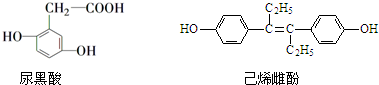
| A�� | ��������������̼ԭ��һ������ͬһƽ���� | |
| B�� | ��ϩ�Ʒӿɷ����ӳɡ�ȡ�����������Ӿۡ�������Ӧ | |
| C�� | �����ͼ�ϩ�ƷӶ����ڷ����廯���� | |
| D�� | ��1mol�������ͼ�ϩ�Ʒӷֱ����������3mol ��6mol Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=5��NH4Cl��Һ�������Һ�У���ˮ������� c��H+����Ϊ10-9mol•L-1 | |
| B�� | �����£���pH=3�Ĵ����pH=11��NaOH��Һ�������Ϻ�pH��7 | |
| C�� | ��c��H+����c��OH-��=1��l012����Һ�У�Na+��I-��NO3-��SO42-�ܴ������� | |
| D�� | 0.1 mol•L-1 Na2CO3��Һ��0.1 mol•L-1 NaHSO4��Һ�������ϣ���Һ�У�c��Na+��+c��H+��=c��CO32-��+c��SO42-��+c��HCO3-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
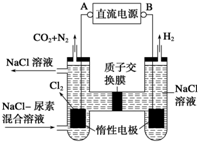
| A�� | A ��Ϊ��Դ�ĸ��� | |
| B�� | �������з����ķ�Ӧֻ��CO��NH2��2-6e-+6OH -=N2��+CO2��+5H2O | |
| C�� | ��������Һ�� PH ���ǰ�ֲ��� | |
| D�� | ��ȥ 3.6 ������ʱ����һ������ H26.72L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | D�Ƿǽ�������ǿ��Ԫ�� | |
| B�� | B�ĵ����ж���ͬ���칹�壬����һ������Ȼ�������Ӳ������ | |
| C�� | B���⻯����ȶ��Դ���D���⻯�� | |
| D�� | A��Cֻ�ܹ��γ����ֻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
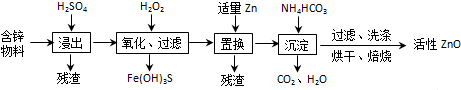
| A�� | ���������У�����ʱ�õ���60% H2SO4���ܶ���1.5g/cm3����������100 mL����H2SO4��Һ������Ҫ18.4mol•L-1��Ũ����ԼΪ49.9mL | |
| B�� | �����ɵij�������̬��ΪZna��OH��b ��CO3��c�ģ�a��b��c���������������ּ�ʽ̼��п�Ļ�����ֱ������Zn5��OH��6��CO3��2 ��Zn3��OH��6CO3 | |
| C�� | ������NH4HCO3�����ɵij�����Zn5��OH��6��CO3��2����÷�ӦΪ5ZnSO4+10NH4HCO3�TZn5��OH��6��CO3��2��+5��NH4��2SO4+8CO2��+2H2O | |
| D�� | ����������H2O2��ֻ��Fe��OH��3�������֣�����Һ��c��Fe3+���T2.6��10-15mol•L-1������Һ��c��Cu2+����2.2��10-4mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | ||
| C�� | 2-�����飨CH3��3CH | D�� | 2��2-�������飨CH3��4C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
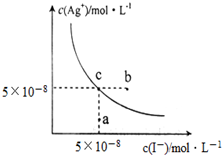 ��t��ʱ��AgI��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgBr��Ksp=5��10-13������˵������ȷ���ǣ�������
��t��ʱ��AgI��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgBr��Ksp=5��10-13������˵������ȷ���ǣ�������| A�� | ��t��ʱ��AgI��Ksp=2.5��10-15 mol2•L-2 | |
| B�� | ͼ��b���е⻯���������� | |
| C�� | ��c����Һ�м�����������ˮ����ʹ��Һ��c�㵽a�� | |
| D�� | ��t��ʱ����ӦAgBr��s��+I-��aq��?AgI��s��+Br-��aq�� ��ƽ�ⳣ��K=200 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com