
| A. | 7 种 | B. | 6 种 | C. | 5 种 | D. | 4 种 |
分析 有机物X为酯,水解得到酸Y和醇Z,Y能使溴的CCl4溶液褪色,说明Y含有一个碳碳双键,能与NaHCO3溶液反应,说明Y含有-COOH,且Y分子中只含有一个甲基,以此分析Y可能的结构简式.
解答 解:有机物X为酯,在稀硫酸中加热条件下水解得到酸Y和醇Z,Y能使溴的CCl4溶液褪色,说明Y含有一个碳碳双键,能与NaHCO3溶液反应,说明Y含有-COOH,且Y分子中只含有一个甲基,满足含有一个碳碳双键、一个-COOH、一个甲基的Y可能是:
①CH3-CH=CH-COOH、CH2=C(CH3)COOH;分子式为C4H6O2,则Z为乙醇,Y与乙醇反应得到两种X;
②在①中插入一个碳原子可得:CH3-CH2-CH=CH-COOH、(CH3)2C=CH-COOH、CH3-CH=CH-CH2-COOH、CH2=C(CH3)-CH2-COOH、CH2=C(CH2CH3)COOH;分子式为C5H8O2,则Z为甲醇,与甲醇反应得到5种X,
因此X最多为7种,
故选A.
点评 本题考查同分异构体的书写,通过性质判定含有的官能团,通过碳链异构和位置异构确定有机物种数,题目难度中等.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
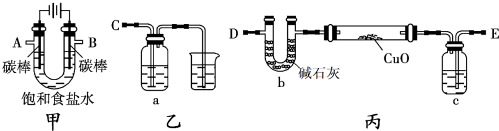
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
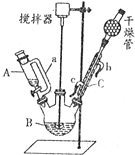 丙烯酸乙酯(CH2═CHCOOCH2CH3,密度为0.94g/mL)可广泛用于涂料、粘合剂的制造、皮革加工等方面.某实验小组利用如图所示的装置合成丙烯酸乙酯(部分夹持及加热装置已省略).
丙烯酸乙酯(CH2═CHCOOCH2CH3,密度为0.94g/mL)可广泛用于涂料、粘合剂的制造、皮革加工等方面.某实验小组利用如图所示的装置合成丙烯酸乙酯(部分夹持及加热装置已省略).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 硫酸工业的生产工艺流程可简略表示如下:
硫酸工业的生产工艺流程可简略表示如下: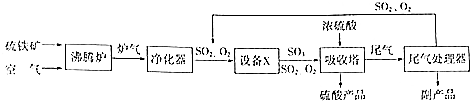 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
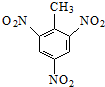 的系统命名:2,4,6-三硝基甲苯;
的系统命名:2,4,6-三硝基甲苯;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com